Активность - карбонильная группа
Cтраница 1
Активность карбонильной группы определяется величиной положительного заряда на атоме углерода, а в карбоксильной группе положительный заряд атома углерода в значительной мере погашен за счет сопряжения со свободными электронными парами гидроксильного кислорода. Под влиянием гидроксильной группы карбонильная группа теряет свою склонность вступать в реакции с нуклеофильными реагентами. [1]
Активность карбонильной группы определяется величиной положительного заряда на атоме углерода, а в карбоксильной группе положительный заряд атома углерода в значительной мере погашен за счет сопряжения со свободными электронными парами гидроксильного кислорода. [2]
Активность карбонильной группы определяется величиной положительного заряда на атоме углерода, а в карбоксильной группе положительный заряд атома углерода в значительной мере погашен за счет сопряжения со свободными электронными парами гидроксильного кислорода. Под влиянием гидроксильной группы карбонильная группа теряет способность вступать в реакции с ну-клеофильными реагентами. [3]
По активности карбонильной группы сложные эфиры заметно уступают альдегидам и кетонам и по этой причине, как правило, неспособны вступать в перечисленные выше реакции, в том числе и конденсироваться с нитросоединениями. [4]
Действительно, активность карбонильной группы формальдегида в отношении типичных карбонильных реакций ни в малейшей степени не мошет быть сравнима с активностью ее в ацетоне. В уксусном ангидриде она совсем мало активна, а в ацетамиде или еще более в мочевине ее совсем не видно. [5]
 |
Строение карбонильной группы, определяющее ее взаимодействие с нуклеофильными реагентами. [6] |
В кислой среде активность карбонильной группы, как правило, увеличивается, поскольку вследствие протонирования атома кислорода на атоме углерода возникает полный положительный заряд. [7]
Это находит отражение в активности карбонильной группы. Уксусная кислота, например, не реагирует с дисульфитом натрия, а уксусный альдегид и ацетон легко образуют соответствующие аддукты ( см. разд. [8]
Сложные зфиры, в которых активность карбонильной группы повышена введением злектроноакцепторных групп ( например, эфиры цианоуксусной и хлороуксусной кислот), вступают в реакцию аммонолиза особенно легко. Группы с - / - эффектом, находящиеся в спиртовом компоненте эфира, также повышают их активность. [9]
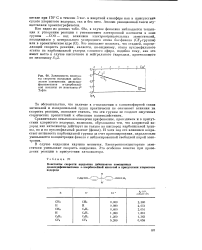 |
Зависимость константы скорости ацидолиза дибен-зоатов замещенных диоксиди-фенилметанов п-хлорбензой-ной кислоты от константы сз Тафта. [10] |
И хотя под его влиянием возрастает активность карбонильной группы за счет протонирования, параллельно уменьшается концентрация фенола с неблокированной свободной парой электронов. [11]
Расположите приводимые ниже соединения в ряд по возрастающей активности карбонильной группы: а) ацетофенон, б) n - нитробензальдегид, в) 2 4-динитробензальдегид, г бенз-альдегид, д) n - хлорбензальдегид, е) п-оксиацетофенон. [12]
Расположите приводимые ниже соединения в ряд по возрастающей активности карбонильной группы: а) ацетофе-нон, б) л-нитробензальдегид, б) 2 4-динитробензальдегид, г) бензальдегид, б) я-хлорбензальдегид, е) п-гидроксиацето-фенон. [13]
Расположите приводимые ниже соединения в ряд по возрастающей активности карбонильной группы: а) ацетофенон; б) л-нитробензальде-гид; в) 2 4-динитробензальдегид; г) бензальдегид; д) л-хлорбензальдегид, е) л-гидроксиацетофенон. [14]
Аналогичные явления имеют место в щелочной среде, так как здесь активность карбонильной группы уменьшается за счет присоединения к ней иона НО9, тогда как основность реагента при этом часто возрастает, например в случае спиртов. [15]
Страницы: 1 2