Поверхностная активность - органическое вещество
Cтраница 1
 |
Химический состав отбеливающих земель ( в %. [1] |
Поверхностная активность органических веществ, как известно, определяется химической структурой их молекул. [2]
Поверхностная активность органических веществ на границе раствор / воздух определяется только эффектом выжимания, который в свою очередь при малых значениях Да зависит от соотношения энергий взаимодействия молекул органического вещества с молекулами растворителя и молекул растворителя друг с другом. [3]
 |
Ориентация полярных молекул при адсорбции в поверхностном слое на разделе двух фаз. [4] |
Установлено, что поверхностная активность органических веществ определяется химической структурой их молекул. Молекулы поверхностно-активных веществ состоят из полярной ( активной) и неполярной ( инактивной) групп. НеполярйЬми группами являются радикалы предельных углеводородов. [5]
Познакомимся с механизмом поверхностной активности органических веществ на примере моющих свойств мыла ( см. разд. [6]
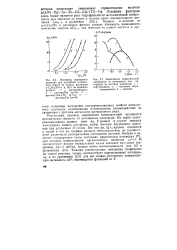
Рассмотрим, наконец, зависимость поверхностной активности органических веществ от потенциала электрода. Все эти Асг, lgCA - кривые относятся к одной и той же границе раздела металл / раствор, но соответствуют различным электрическим состояниям системы. [8]
Лэнгмюр и Гаркинс независимо друг от друга показали, что поверхностная активность органических веществ определяется химическим строением их молекул. Такие молекулы отличаются несимметричным строением и состоят из двух различных частей, они полярны и дифильны. В такую молекулу входит неполярная ( инактивная) группа - углеводородная цепь и полярная ( активная) группа - радикал или группа атомов с ненасыщенными химическими валентностями. Сюда относятся группы ОН, СООН, CN, SH, NH2, двойная связь и др. Эти сильно полярные группы, создавая силовое поле, проявляют средство к полярной фазе, воде, полярные группы обращаются при этом к водной фазе, а неактивная углеводородная цепь выталкивается из нее, обращаясь к менее полярной фазе. Оси адсорбированных молекул стремятся ориентироваться перпендикулярно к поверхности раздела. [9]
Однако, если атомы водорода в молекулах этих соединений замещены атомами галоидов, то ситуация резко изменяется. Так, замена Н на F приводит к тому, что поверхностная активность органического вещества оказывается выше на границе раствор / воздух, а замена Н на С1, Вг или I приводит, наоборот, к более высокой поверхностной активности на границе раствор / ртуть, причем эффект возрастает при переходе от хлора к брому и далее к йоду. Полученные результаты указывают на то, что специфическое взаимодействие с поверхностью ртути растет в ряду: CF CHCClCBrCI. Причиной этого является усиление в том же ряду донорно-акцепторного взаимодействия между органической молекулой и поверхностью ртути, при котором электроны с атомов С1, Вг и I могут переходить на уровни зоны проводимости металла. [10]
Как известно из электрокапиллярных измерений [30], усиление адсорбции органических веществ при высокой концентрации индифферентного электролита происходит лишь в ненасыщенных растворах поверхностно-активных веществ, а в случае насыщенных растворов изменение ионной силы раствора не влияет на адсорбцию. Такая связь между адсорбцией и концентрацией постороннего электролита была объяснена повышением поверхностной активности органического вещества при увеличении и он но и силы раствора в результате высаливающего действия соли на органическое вещество. [11]
Более сложная картина наблюдается для ароматических и гетероциклических соединений, адсорбция которых может сопровождаться л-электронным взаимодействием с поверхностью металла. Такому взаимодействию естественно благоприятствует наличие положительных зарядов на поверхности электрода и, наоборот, при достаточно большом отрицательном заряде поверхности в результате отталкивания л-электронов происходит изменение ориентации адсорбированных органических молекул. Таким образом, поверхностная активность органических веществ, молекулы которых обладают системой сопряженных л-электронных связей, характеризуется наличием двух адсорбционных состояний. Эту особенность и отражает кривая 3 на рис. 2.7, состоящая из двух участков, каждый из которых дает зависимость - АС от Е для соответствующей ориентации молекул адсорбата. [12]
Поверхностная активность органических соединений в более сильно поляризующемся, по сравнению с октаном, бензоле резко снижается [32], и соответственно этому деформационная активность растворов поверхностно-активных веществ в бензоле ниже, чем в октане. В полярном растворителе - воде - деформационная активность поверхностно-активных веществ резко снижается. Это снижение энергии взаимодействия адсорбированных молекул с поверхностью металла вполне соответствует тому, что поляризация в воде полярных групп и их гидратация [31 ] значительно снижают поверхностную активность органических веществ в водных растворах. [13]
Страницы: 1