Высокая антихолинэстеразная активность
Cтраница 1
Высокая антихолинэстеразная активность этого неопентильного производного, вероятно, и объясняется тем, что анионный пункт ХЭ окружен объемистым гидрофобным участком, на котором и сорбируется mpm - бутиль-ная группировка этого ФОИ, подобно сорбции триметиламмониевой группы АХ. [1]
При высокой антихолинэстеразной активности фосфорорга-нические соединения в разной степени ядовиты для человека и теплокровных животных. Некоторые из них относятся к числу сильнодействующих веществ, другие - к высокотоксичным или среднетоксичным пестицидам. [2]
Чтобы соединение обладало высокой антихолинэстеразной активностью, должна происходить не только быстрая реакция между ферментами и фосфатом, но и фосфорнлированный фермент должен быть стабилен к гидролизу. [3]
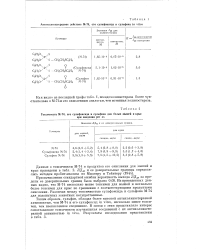 |
Антихолинэстеразное действие М-74, его сульфоксида и сульфона in vitro. [4] |
Таким образом, сульфон, обладая более высокой антихолинэстеразной активностью, чем М-74 и его сульфоксид in vitro, несколько менее токсичен, чем неокисленное соединение. [5]
Наиболее отчетливо этот параллелизм проявляется у соединений, обладающих высокой антихолинэстеразной активностью. У соединений же с низкой антихолинэстеразной активностью подобный параллелизм отсутствует. [6]
Между величиной антихолинэстеразного эффекта и токсичностью для мышей отчетливый параллелизм проявляется только у соединений, обладающих высокой антихолинэстеразной активностью. У соединений с низкой антихолинэстеразной активностью подобный параллелизм отсутствует. [7]
Он был синтезирован в среде органического растворителя, но была также показана возможность его образования в более физиологических условиях, а именно в водном растворе ( рН 7 6) при комнатной температуре при взаимодействии Ю-4 М 4 - ПАМ с 10 - 2 М зарина. Этот 4 - ФПАМ обладает в 1 4 раза более высокой антихолинэстеразной активностью, чем зарин. [8]
Зависимость инсектицидной и антихолинэстеразной активности карбаматов от их строения имеет более сложный характер, чек указано выше, и пока еще недостаточно изучена. Несомненно, что, кроме гидролитической стабильности карбаматов, для наличия у них высокой антихолинэстеразной активности необходимо определенное пространственное расположение молекулы или ее части по отношению к соответствующим активным центрам эсте-разы. [9]
Зависимость инсектицидной и антихолинэстеразной активности карбаматов от их строения имеет более сложный характер, чем указано выше, и пока еще недостаточно изучена. Несомненно, что, кроме гидролитической стабильности карбаматов, для наличия у них высокой антихолинэстеразной активности необходимо определенное пространственное расположение молекулы или ее части по отношению к соответствующим активным центрам эстеразы. [10]
При метаболизме в листьях хлопчатника 14С - карбофуран претерпевает, как и в листьях табака и капусты, в основном окислительное гидроксилирование углеродного атома гидрированного фуранового цикла с образованием 3-оксипроизводного ( см. схему на с. При метаболизме протекает также гидролиз N-метилкарбаматов и получаются различные фенолы ( см. схему), которые образуют далее конъюгаты с глюкозой. Продукты окисления карбофурана сохраняют высокую антихолинэстеразную активность. Как и в случае карбарила, метаболизм карбофурана в животных и растениях сходен в общих чертах. [11]
Резюмируя сказанное, следует отметить, что данных по изучению механизма действия инсектицидов на нервную систему насекомых недостаточно для того, чтобы точно указать, как действуют различные инсектициды п как именно происходит нарушение передачи нервных импульсов у насекомых. Почти все виды инсектицидов оказывают прямо или косвенно токсическое действие на нервную систему насекомых. Несомненно, представление о том, что высокая антихолинэстеразная активность фосфорорганическпх соединений и карбаматов является признаком их высокой инсектицидной активности, сейчас уже устарело и не может быть ведущим при отборе новых инсектицидов. Эта зависимость прослеживается только частично для отдельных групп соединений и отдельных объектов и не подтверждается для других. [12]
Порядок активности, за исключением триметиламмониевой группы, указывает, что антихолинэстеразная активность является функцией способности заместителя отдавать электроны N-метилкарбамоильной части молекулы. Увеличение электронной плотности вокруг карбони-ла делает молекулу более устойчивой к гидролизу. В противоположность фосфорорганическим соединениям одним из требований к структуре карбаматов для высокой антихолинэстеразной активности является устойчивость к гидролизу, и, таким образом, кар-баматы ведут себя, как конкурирующие ингибиторы, а не субстраты холинэстеразы. В дополнение к гидролитической стабильности другим важным требованием к строению для высокой антихолинэстеразной активности является соответствующее расположение молекулы на поверхности фермента активной стороной и способность блокировать нормальную реакцию субстрата. Этому требованию частично удовлетворяет N-метилкарбамоильная часть, которая, по-видимому, притягивается к эфирной части теми же силами, которые связывают ацетоксильную часть молекулы ацетилхолина. Это очевидно из данных Кольбецена, на основании которых соединения, обладающие устойчивой неизмененной N-метилкарбамоильной частью молекулы, являются в различной степени ингибиторами холинэстеразы. Кроме того, антихолинэстеразная активность может быть увеличена введением заместителей в орто - и лета-положения, например лг-диметиламино -, ж-изопропил -, о - и л-бутилгруппы, которые в пространственном отношении напоминают триметилам-мониевую группу ацетилхолина. [13]
Порядок активности, за исключением триметиламмониевой группы, указывает, что антихолинэстеразная активность является функцией способности заместителя отдавать электроны N-метилкарбамоильной части молекулы. Увеличение электронной плотности вокруг карбони-ла делает молекулу более устойчивой к гидролизу. В противоположность фосфорорганическим соединениям одним из требований к структуре карбаматов для высокой антихолинэстеразной активности является устойчивость к гидролизу, и, таким образом, кар-баматы ведут себя, как конкурирующие ингибиторы, а не субстраты холинэстеразы. В дополнение к гидролитической стабильности другим важным требованием к строению для высокой антихолинэстеразной активности является соответствующее расположение молекулы на поверхности фермента активной стороной и способность блокировать нормальную реакцию субстрата. Этому требованию частично удовлетворяет N-метилкарбамоильная часть, которая, по-видимому, притягивается к эфирной части теми же силами, которые связывают ацетоксильную часть молекулы ацетилхолина. Это очевидно из данных Кольбецена, на основании которых соединения, обладающие устойчивой неизмененной N-метилкарбамоильной частью молекулы, являются в различной степени ингибиторами холинэстеразы. Кроме того, антихолинэстеразная активность может быть увеличена введением заместителей в орто - и лета-положения, например лг-диметиламино -, ж-изопропил -, о - и л-бутилгруппы, которые в пространственном отношении напоминают триметилам-мониевую группу ацетилхолина. [14]
Страницы: 1