Фунгицидная активность - соединение
Cтраница 2
По результатам табл. 2 можно видеть, что удлинение радикала, находящегося в положении 2 бензимидазольного кольца, в основном, не увеличивает фунгицидной активности соединения. [16]
Исследование фунгицидной активности соединений в отношении мучнистой росы огурцов и стеблевой ржавчины пшеницы проводилось в тепличных условиях на растениях огурцов сорта Клинские тепличные и растениях пшеницы сорта Краснозеряая при искусственном заражении. [17]
Исследование фунгицидной активности соединений в отношении мучнистой росы огурцов и стеблевой ржавчины пшеницы проводилось в тепличных условиях на растениях огурцов сорта Клинские тепличные и растениях пшеницы сорта Краснозерная при искусственном заражении. [18]
Ртутноорганические соединения алифатического ряда являются сильными фунгицидами, а соединения ароматического ряда - бактерицидами. Введение в алифатический радикал функциональных групп изменяет фунгицидную активность соединения. Так, при введении в положение 2 метоксильной группы фунгицидность соединения уменьшается незначительно, а при введении карбонильной группы - более сильно. Для соединений ароматического ряда введение функциональных групп в ароматический радикал, связанный со ртутью, также оказывает влияние на их токсичность как для микроорганизмов, так и для животных. Наибольшей активностью обладают фенил - и толилпроизводные. Увеличение молекулярного веса углеводородного радикала снижает активность препарата. Полициклические производные ртути менее активны. [19]
Фунгитоксичность нерастворимых в, воде солей алкил - и диал-килдитиокарбаминовых кислот уменьшается с увеличением количества атомов углерода в алкильных радикалах. Введение ароматического радикала к азоту иногда повышает фунгицидную активность соединения или избирательность действия препарата на те или иные виды грибов. [20]
Соединения ( 45), содержащие при экзоциклическом азоте алифатический радикал, недостаточно стабильны и практического применения не находят. При замене этого алифатического радикала на ароматический фитоцилность уменьшается и возрастает фунгицидная активность соединения. Наиболее активен 2 4-дихлор - 6 - ( 2-хлорфениламино) - 1 3 5-триазин ( препарат анилазин, см. ниже), который в небольших масштабах используется для борьбы с болезнями растений. Его изомеры, содержащие галогены в других положениях ароматического ядра, менее активны. [21]
Соединения ( 45), содержащие при экзоциклическом азоте алифатический радикал, недостаточно стабильны и практического применения не находят. При замене этого алифатического радикала на ароматический фитоцидность уменьшается и возрастает фунгицидная активность соединения. Наиболее активен 2 4-дихлор - 6 - ( 2-хлорфениламино) - 1 3 5-триазин ( препарат анилазин, см. ниже), который в небольших масштабах используется для борьбы с болезнями растений. Его изомеры, содержащие галогены в других положениях ароматического ядра, менее активны. [22]
Бензохиноны проявляют относительно невысокое фунгицид-ное действие, но при введении в бензольное кольцо галогенов, углеводородных радикалов, амино - и ациламиногрупп активность соединений значительно возрастает. Дальнейшее накопление атомов хлора в молекуле нафтохинона-1 4 приводит к снижению фунгицидной активности соединения. [23]
Соединения общей формулы XII, содержащие при нециклическом азоте алифатический радикал, недостаточно стабильны и практического применения не находят, хотя и обладают гербицид-ными свойствами. При замене этого алифатического радикала на ароматический фитоцидные свойства уменьшаются и возрастает фунгицидная активность соединения. Наиболее активен 2 4-дихлор - 6 - ( 2 -хлорфениламино) - силш-триазин ( дирен), который используется для борьбы с болезнями растений. Его изомеры, содержащие галоген в других положениях, менее активны. [24]
Одновременно с увеличением токсичности для насекомых повышается и фитотоксичность. При введении в молекулу алифатического тиоцианата различных функциональных групп часто повышается не только инсектицидная, но и фунгицидная активность соединения. Наиболее активными атомами и группами являются галоиды, вторая родангруппа, сульфидная и сложно-эфирная группировки. [25]
После выдержки в течение 18 - 20 часов агаровую поверхность просматривают при малом увеличении микроскопа и подсчитывают количество проросших ( или непроросших) спор. Иногда глазомерно отмечают наличие или отсутствие роста гриба в чашке. В этом случае фунгицидная активность соединений характеризуется величиной минимальной концентрации, обеспечивающей полное подавление роста сриба. [26]
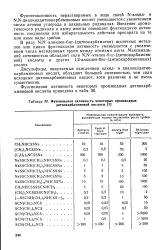 |
Фунгицидная активность некоторых производных дитиокарбаминовой кислоты. [27] |
N-диалкилдитиокарбаминовых кислот уменьшается с увеличением числа атомов углерода в алкильных радикалах. Введение ароматического радикала к азоту иногда повышает фунгицидную активность соединения или избирательность действия препарата на те или иные виды грибов. [28]
Тиоцианаты с разветвленным алкильным остатком обладают меньшей инсектицидной активностью, чем соединения с нормальным строением углеродной цепи того же молекулярного веса. Введение в молекулу тиоцианата различных функциональных групп и атомов галогенов несколько увеличивает активность соединения. При этом одновременно с увеличением токсичности для насекомых повышается и фитотоксичность. При введении в молекулу алкилтиоцианата различных функциональных групп часто повышается не только инсектицидная, но и фунгицидная активность соединения. Наиболее сильно повышается активность при введении атомов галогенов, второй тиоцианатогруппы, алкилмер-капто - и сложноэфирной групп. [29]
Марш и Бутлер [71, 72] систематически изучали несколько таких соединений и установили, что фунгицидная активность их зависит от характера связи между двумя фенольными группами в молекуле. Одни типы связей благоприятны для активности, другие не благоприятны. Содержащие кислород связи ( - SO, - SO2 -, - СО-СО -) снижают фунгицидную активность, а бескислородные ( - CHg -, - СНСН -, - СН ( СНз) -) повышают ее. Наличие боковых цепей или блокирование фенольных групп существенно снижает фунгицидную активность соединений. Из диоксидифенильных производных самой большой эффективностью обладает 2 2 -диокси - 5 5 -дихлордифенилметан. [30]
Страницы: 1 2