Электрофильная активность
Cтраница 2
 |
Гидролиз ацетилсиликата при 20. [16] |
В отличие от этилсиликата, это соединение обладает двумя конкурирующими центрами электрофильной активности - кремнием и карбонильным углеродом. Реакция гидролиза ацетилсиликата протекает практически мгновенно на границе твердой и жидкой фаз и сопровождается бурным разогреванием. Полученная при гидролизе уксусная кислота превращалась в ацетат серебра. [17]
Принципиально иной подход к синтезу макроциклических лиган-дов типа VII основан на высокой электрофильной активности 1 2-дитиолиевых катионов в реакциях с диаминами. [18]
Замена у кремния атомов галоида на метальные группы приводит к снижению его электрофильной активности, и реакция отщепления не протекает. [19]
Так как преобладает структура I, положительный заряд на крайнем атоме азота невелик и электрофильная активность соединения в реакции сочетания мала. [20]
Таким образом, нуклеофильная активность этиленовой двойной 1 связи проявляется предпочтительно по сравнению с электрофильной активностью, которая проявляется лишь во второй стадии. То, что подобные отношения действительно имеют место, можно доказать кинетическими исследованиями, а Также тем фактом, что реакция ускоряется при повышении концентрации ионов водорода. Повышение же концентрации анионов брома не влияет на скорость реакции. [21]
Поскольку преобладает структура ( 9), положительный заряд на крайнем атоме азота невелик и электрофильная активность соединения в реакции сочетания мала. [22]
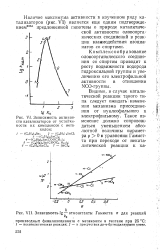 |
Зависимость активно. [23] |
Комплексообразование оловоорганического соединения со спиртом приводит к росту подвижности водорода гидроксильнои группы и увеличению его электрофильной активности в отношении NCO-группы. [24]
Это можно объяснить отрицательным индуктивным эффектом ( - 7) атомов хлора, которые увеличивают электрофильную активность карбонильных групп. [25]
В результате того, что положительный заряд катиона Манниха делокализован между атомами углерода и азота, электрофильная активность этого катиона гораздо выше, чем у незаряженного азометина, соответствуя примерно активности формальдегида. Поэтому к катиону относительно легко могут присоединяться даже слабо нуклеофильные вещества типа кетонов. Механизм реакции при этом отвечает катализируемому кислотами альдольному присоединению. В согласии с этим реакция Манниха с высшими метилкетонами идет не по метальной, а по метиленовой группе ( см. также разд. [26]
Последовательность расположения групп X в случае Swl-процессов симбатна устойчивости электрофила Х в растворе; другими словами-чем ниже электрофильная активность Х, тем легче отщепляется группа X при Swl-распаде аренониевого иона. Сопоставление легкости отщепления групп, принадлежащих к разным рядам, осложняется влиянием нуклеофильности среды на процессы 5к2 - типа ( ср. [27]
Алкоголят алюминия [ схема ( 420, / /) ], являясь кислотой Льюиса, повышает электрофильную активность карбонильной группы. Одновременно частично положительно заряженный, комплексно связанный атом алюминия вызывает сдвиг электронов в исходящих от него связях. [28]
Если в качестве второго компонента применяют карбонильные соединения типа изатина ( 17), то реакция идет по В-карбонильной группе, электрофильная активность которой выше, так как заряд на - атоме углерода снижается под влиянием соседней имино-группы или енольной гидроксигруппы. [29]
Такая специфическая сольватация ведет к снижению свободной энергии молекул и особенно ионов, что существенно сказывается на скоростях реакции, на нуклеофильной или электрофильной активности реагентов и реакционной способности веществ. При этом специфическая сольватация может вызвать изменение скорости на 8 - 9 порядков по сравнению с 2 - 3 порядками при электростатической сольватации. [30]
Страницы: 1 2 3