Электрохимическая активность
Cтраница 3
Наибольшей электрохимической активностью обладает поверхность, обработанная песком, диаметр частиц которого 0 20 мм. На такой поверхности образуется мелкокристаллическая плотная фосфатная пленка с высокими защитными свойствами. Худшие результаты получены при большей шероховатости поверхности: обработка металла песком с диаметром частиц 0 80 мм способствовала образованию неоднородной фосфатной пленки с низкими защитными свойствами. Наихудшие результаты получены при электролитической полировке поверхности, в этом случае образовалась крупнокристаллическая пленка. Полированная поверхность обладает наименьшей электрохимической активностью и малым числом центров кристаллизации, что и способствует образованию крупнокристаллической коррозионно-нестойкой пленки. Пескоструйная обработка полностью депассивирует поверхность и увеличивает на ней число центров кристаллизации. [31]
Исследована электрохимическая активность а - и Р - РЬО2 в растворах кремнефтористоводородной кислоты. [32]
Поэтому электрохимическая активность гидрофобизированного электрода, в котором имеются только поры типа II, практически не зависит от газовой пористости. [33]
Исследована электрохимическая активность дисперсных сплавов палладий - платина в реакциях выделения и ионизации водорода и ионизации кислорода в кислых и щелочных растворах. [34]
 |
Свойства металлов II группы побочной подгруппы. [35] |
По электрохимической активности цинк превосходит кадмий. Нормальный потенциал цинка - 0 76 В, а кадмия - 0 402 В; цинк вытесняет кадмий из его солей. [36]
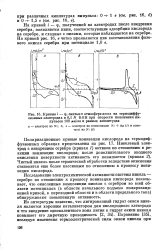 |
Кривые i - ф, снятые в атмосфере азота на термодиффузионных электродах в 0 1 Л КОН при скорости наложения импульсов 100 мв / сек и разных амплитудах. [37] |
Исследование электрохимической активности системы никель - серебро по отношению к процессу ионизации кислорода показывает, что окисленные композиции никеля с серебром во всей области потенциалов ( в области начального подъема поляризационной кривой, в переходной области и в области предельного тока) обнаруживают повышенную активность. [38]
О высокой электрохимической активности магния свидетельствует отрицательное значение его равновесного стандартного потенциала ( - 2 364 В), что лишь на 0 3 В положительнее равновесного потенциала натрия. Стационарные потенциалы магния в большинстве водных растворов также отрицательны для технических металлов и могут доходить до - 1 64 В. Лишь в пассивирующих для магния растворах потенциал может быть положительным. С течением времени потенциалы магния и его сплавов, как правило, смещаются в положительную сторону вследствие постепенного пассивирования поверхности. [40]
 |
Схема прибора для определения обменной способности мембран в процессе электродиализа. [41] |
Селективность или электрохимическая активность выражается в способности мембраны, помещенной в растворе электролита в электрическое поле, изменять числа переноса ионов. Выход по току в процессе электродиализа определяется числами переноса ионов в мембране. [42]
УФ-поглощение или электрохимическая активность пробы мала или полностью отсутствует. Изменив состав ионообменной жидкой мембраны, можно получить электрод, чувствительный к большому числу органических анионов и катионов. [43]
Устойчивость и высокая электрохимическая активность стабильных анодов, как правило, обусловливаются образованием на их поверхности оксидов различного состава. [44]
По характеру электрохимической активности ненасыщенные соединения могут быть разбиты на три основные группы. [45]
Страницы: 1 2 3 4 5
