Малая химическая активность
Cтраница 3
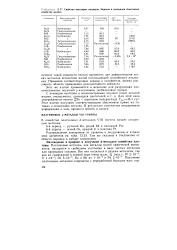 |
Свойства некоторых нитридов, боридов и силицидов ( ( - металлов семейства железа. [31] |
Платиновые металлы, как металлы малой химической активности, находятся в свободном состоянии в виде чистых металлов или природных сплавов. Все они относятся к редким металлам, так как их содержание в земной коре очень мало, % ( мае. [32]
Платиновые металлы, как металлы малой химической активности, находятся в свободном состоянии - в виде чистых металлов или природных сплавов. Получение платиновых металлов сопряжено с переработкой больших масс горных пород, а затем со сложными химическими процессами разделения этих металлов. [33]
В тампонажных материалах на оксидной основе расширение происходит в ходе кристаллизации труднорастворимых гидрооксидов Са и Mg. Высокая температура обжига клинкера обусловила малую химическую активность этих оксидов, поэтому они при твердении в условиях низких температур вызывают внутреннее напряжение на поздних стадиях твердения, когда пластичность цементного камня недостаточна. Поэтому расширение, вызванное оксидами кальция и магния, сопровождается трещинообразованием и снижением прочности цементного камня. [34]
Предельные углеводороды называют также парафинами. Смысл этого слова состоит в их малой химической активности. Их называют еще углеводородами жирного ряда, так как производные некоторых высших углеводородов этого ряда являются жирами. [35]
Различают две группы коррозионностойких металлов. Одни металлы хорошо сопротивляются коррозии вследствие их малой химической активности. Другие же, являясь по своей природе активными элементами, приобретают высокую химическую устойчивость благодаря явлению пассивности. К первой группе относятся платина, палладий, золото, ко второй - хром, титан, алюминий и др. Для увеличения коррозионной стойкости химически активного металла в него вводят легирующие элементы. [36]
Различают две группы корро-зионностойких металлов. Одни металлы хорошо сопротивляются коррозии вследствие их малой химической активности. Другие же, являясь по своей природе активными элементами, приобретают высокую химическую устойчивость, благодаря явлению пассивности. К первой группе относятся платина, палладий, золото, ко второй - хром, титан, алюминий и др. Для увеличения коррозионной стойкости химически активного металла в него вводят легирующие элементы. [37]
В симметричных октаэдрических молекулах шестифтористых соединений полярность отдельных связей полностью компенсируется и дипольный момент молекул равен нулю. Экранирование центральных атомов шестью атомами фтора приводит к малой химической активности этих веществ. Особо химически устойчива шестифтористая сера. Эти вещества обладают заметным сходством и с гексафторидами переходных элементов не только шестой, но и VII и VIII групп периодической системы. [38]
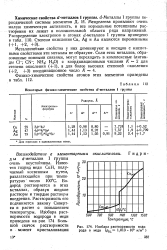 |
Изобара растворимости водорода в меди ( рНз 1 013 105 и / ж2. [39] |
Металлы I группы периодической системы элементов Д. И. Менделеева проявляют очень малую химическую активность, и все нормальные потенциалы растворения их лежат в положительной области ряда напряжений. [40]
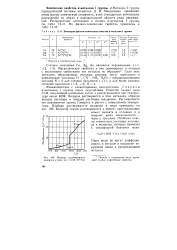 |
Некоторые физико-химические свойства d - металлов I группы. [41] |
Металлы I группы периодической системы элементов Д. И. Менделеева проявляют очень малую химическую активность, и все стандартные потенциалы растворения их лежат в положительной области ряда напряжений. [42]
Для промысловых испытаний были рекомендованы неионогенные ПАВ ( НПАВ), обладающие наименьшей адсорбцией. Лабораторные исследования и промышленные испытания доказали с позиций физико-химической термодинамики слишком малую химическую активность НПАВ типа ОП-10 по отношению к высоким энергиям межмолекулярных взаимодействий на границе нефть - порода и поверхностной энергии на границе нефть - вода, которые определяют отрыв и перенос глобул нефти в нефтевытесняющем потоке. [43]
Золото - электроположительный металл, его равновесный потенциал для процесса Ag - Ag3 ЗЭ равен 1 5 в. Высокая коррозионная стойкость золота зависит не от образования пассивной пленки, а от малой химической активности его. Золото разрушается в сильных окислителях, содержащих свободные галогены, например в азотной и соляной кислотах, в серной кислоте и гипохлорате, в соляной кислоте и марганцевокислом калии и др. Однако в смеси азотной и плавиковой кислот золото устойчиво. Чистая соляная кислота не воздействует на золото, но в присутствии кислорода и при нагреве наблюдается сильная коррозия. Золото устойчиво в муравьиной и плавиковой кислотах. Оно растворяется в царской водке и растворе цианистого калия или натрия, быстро разрушается в горячих смесях серной и азотной кислот и серной кислоты с окислами тяжелых металлов. Золото частично растворяется при кипячении в азотной и в серной кислоте в присутствии кислорода при 250 С. Чистое золото стойко в кислороде, сере, сернистом ангидриде и селене. [44]
Электроположительный металл, его равновесный потенциал для процесса Ag - - Ag3 3 e равен 1 5 В. Высокая коррозионная стойкость золота зависит не от образования пассивной пленки, а от малой химической активности его. Золото разрушается в сильных окислителях, содержащих свободные галогены, например в азотной и соляной кислотах, в серной кислоте и гипохлорате, в соляной кислоте и марганцевокислом калии и др. Однако в смеси азотной и плавиковой кислот золото устойчиво. Чистая соляная кислота не воздействует на золото, но в присутствии кислорода и при нагреве наблюдают сильную коррозию. Золото устойчиво в муравьиной и плавиковой кислотах. Оно растворяется в царской водке и растворе цианистого калия или натрия, быстро разрушается в горячих смесях серной и азотной кислот и серной кислоты с окислами тяжелых металлов. Золото частично растворяется при кипячении в азотной и серной кислотах в присутствии кислорода при 250 С. Чистое золото стойко в кислороде, сере, сернистом ангидриде и селене. [45]
Страницы: 1 2 3 4