Значительная химическая активность
Cтраница 2
Железо, будучи элементом побочной подгруппы VIII группы, проявляет значительную химическую активность, обладает высокой приверженностью к аллотропическим модификациям и пространственно-фазовым превращениям. Железо образует множество соединений как стехиометрического состава, так и бертоллидного характера. Последние играют важную роль при проявлении железосодержащими реагентами коагулирующего и адсорбционного действия. [16]
По своим химическим свойствам скандии относится к металлам и обладает значительной химической активностью. Он быстро тускнеет и окисляется на воздухе, хорошо растворяется в разбавленных минеральных кислотах и медленно разлагает воду при нагревании, выделяя водород. [17]
По своим химическим свойствам скандий относится к металлам и обладает значительной химической активностью. Он быстро тускнеет и окисляется на воздухе, хорошо растворяется в разбавленных минеральных кислотах и медленно разлагает воду при нагревании, выделяя водород. [18]
Одно из последних указаний [3] об умеренной нестабильности красного фосфора дает возможность предполагать значительную химическую активность со многими химическими агентами, в том числе и со щелочами. Так, например, при нормальной температуре и влажности красный фосфор медленно реагирует с парами воды и кислородом воздуха, образуя фосфин и смесь кислородных кислот фосфора. Этот процесс экзотермичен и ускоряется с повышением температуры. [19]
В ряду напряжений рассматриваемые металлы расположены между алюминием и цинком и поэтому должны проявлять значительную химическую активность. Тем не менее, все они при нормальных условиях отличаются высокой химической стойкостью ( устойчивы по отношению к воздуху, воде, растворам кислот и щелочей) благодаря плотной оксидной пленке, образующейся на их поверхности, особенно при действии кислот-окислителей. Ниобий и тантал устойчивы даже в концентрированной азотной кислоте и царской водке. Ванадий на холоду растворяется лишь в царской водке и концентрированной плавиковой кислоте, а при нагревании - в концентрированной азотной и серной кислотах. [20]
В ряду напряжений рассматриваемые металлы расположены между алюминием и цинком и поэтому должны проявлять значительную химическую активность. Тем не менее, все они при нормальных условиях отличаются высокой химической стойкостью ( устойчивы по отношению к воздуху, воде, растворам кислот и щелочей) благодаря плотной оксидной пленке, образующейся на их поверхности, особенно при действии кислот-окислителей. Ниобий и тантал устойчивы даже в концентрированной азотной кислоте и царской водке. Ванадий на холоду растворяется лишь в царской водке и концентрированной плавиковой кислоте, а при нагревании-в концентрированной азотной и серной кислотах. [21]
В ряду напряжений рассматриваемые металлы расположены между алюминием и цинком и поэтому должны проявлять значительную химическую активность. Тем не менее, все они при обычных условиях отличаются высокой химической стойкостью ( устойчивы по отношению к воздуху, воде, растворам кислот и щелочей) благодаря плотной оксидной пленке, образующейся на их поверхности, особенно при действии кислот-окислителей. Ниобий и тантал устойчивы даже в концентрированной азотной кислоте и царской водке. Ванадий на холоду растворяется лишь в царской водке и концентрированной плавиковой кислоте, а при нагревании - в концентрированной азотной и серной кислотах. [22]
Окись бериллия, прокаленная при низких температурах ( 400 - 500 С), обладает значительной химической активностью - легко растворяется в кислотах, труднее - в растворах щелочей. Окись бериллия, подвергнутая нагреванию при температурах выше 1000 С, растворяется лишь во фтористоводородной кислоте, горячей концентрированной серной кислоте, а также при сплавлении с карбонатами, щелочами и пиросульфатами щелочных металлов, причем растворение ее происходит значительно медленнее, чем окиси, прокаленной при невысоких температурах. [23]
Следовательно, для осуществления гомогенно-каталитической реакции рассматриваемого типа необходимо, чтобы сам катализатор как таковой обладал значительной химической активностью. [24]
В ряду напряжений ванадий, ниобий и тантал расположены между алюминием и цинком и поэтому должны проявлять значительную химическую активность. Тем не менее все они при обычных условиях отличаются высокой химической стойкостью ( устойчивы по отношению к воздуху, воде, растворам кислот и щелочей) благодаря плотной оксидной пленке, образующейся на их поверхности, особенно при действии кислот-окислителей. Ниобий и тантал устойчивы даже в концентрированной азотной кислоте и царской водке. Ванадий на холоду растворяется лишь в царской водке и концентрированной плавиковой кислоте, а при нагревании - в концентрированной азотной и серной кислотах. [25]
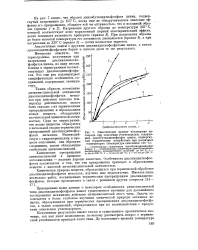
Аппаратом, предназначенным дать весьма быстрое и стандартизованное испытание светонрочности, является ртутно-квар-цевая лампа, ( см. Лампы электрические), которая излучает свет весьма значительной химической активности, отличающийся весьма быстрым действием на красящие вещества. Испытания производятся вместо педель в течение нескольких часов, однако результаты резко отличаются от результатов, получающихся при И. Кроме того лучи кварцевой лампы сильно озонируют воздух, а озон разрушает красящие вещества весьма быстро и поэтому совершенно искажает толкование результатов. Этот инсоляционный прибор представляет собой небольшую эвакуированную кварцевую трубку с ртутью, заключенную в металлич. Более совершенным прибором является получивший в последние годы относительно широкое распространение федометр ( фиг. Вольтова дуга федометра, дающая ( до 3 600, заключена в обычный стеклянный колпак, находящийся в металлическом тамбуре с прорезями, в к-рые вставляются рамочки с наполовину затененными образцами. [26]
Таким образом, повышение антиокислительной активности диалкилдитиофосфатов металлов при действии высоких температур действительно может быть связано с их термическими превращениями и образованием новых веществ, обладающих значительной химической активностью. Судя по термограмме, эти новые вещества образуются в начальной стадии термических превращений диалкилдитиофосфатов металлов. Взаимодействуя с гидроперекисями в процессе окисления, они образуют соединения, также обладающие свойствами антиокислителей. [28]
Железо, кобальт и никель в компактном виде в обычных условиях при отсутствии влаги заметно не реагируют даже с типичными неметаллами - кислородом, серой и галогенами, но проявляют значительную химическую активность в измельченном состоянии при нагревании. [29]
Применение газовой хроматографии для разделения и анализа оксидов азота дает хорошие результаты лишь в тех случаях, когда исследуемые смеси содержат только N2O и NO, поскольку другие оксиды азота, и особенно NO2, отличаются значительной химической активностью. [30]
Страницы: 1 2 3