Актинид
Cтраница 1
Актиниды и лантаниды у нас часто именуют актиноидами и лантаноидами. [2]
Актиниды образуют гидриды общей формулы МН3 ( см. стр. [3]
Актиниды и лантаниды могут быть разделены экстракцией из азотнокислого водного раствора керосиновым раствором три-бутилфосфата. [4]
Актиниды во многих отношениях имеют сходство с лантанидами, так как у обеих групп элементов достраиваются / - оболочки. Так, актиний и лантан являются прототипами соответствующих групп. Хотя актиниды и лантаниды действительно близки во многих важных свойствах, между ними имеются также и существенные отличия. [5]
Актиниды характеризуются тем, что переход от одного элемента к другому осуществляется достройкой электронами глубоко расположенного 5 / - уровня. [6]
Актиниды образуют ионы, подобные ионам редкоземельных элементов. В кислых водных растворах образуется четыре типа катионов. В табл. 9 представлены эти катионы и указана окраска их в водных растворах. [7]
Актиниды в металлическом состоянии, подобно лан-танидам, отличаются высокой электроположительностью. [8]
Актиниды обычно считают исключительно сильными физиологическими ядами, за исключением нескольких изотопов с очень большим периодом полураспада. [9]
Актиниды, так же как и лантаниды, правильнее всего в соответствии с четко выраженной внутренней периодичностью их строения и свойств считать побочным рядом седьмого периода и выносить в две строки, располагая их по соответствующим группам. III группы, и заканчиваются также элементами III группы - галлием, индием, таллием и лютецием. [10]
Актинидов, как и редких земель, должно быть 14, так что их группа должна заканчиваться на элементе с Z-103. Спектры этих элементов, особенно трансурановых, изучены пока слабо, что не позволяет в большинстве случаев с уверенностью установить их наиболее глубокие электронные конфигурации. Тем не менее можно считать установленным, что, как и в случае редких земель, последовательное заполнение f - оболочки электронами имеет место лишь для трехкратных ионов. [11]
Производные пятивалентных актинидов сравнительно мало изучены. [12]
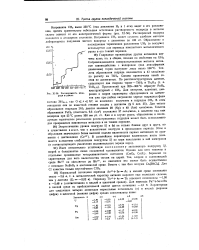 |
Растворимость водорода в уране. [13] |
Гидридные производные других актинидов изучены хуже, но, в общем, похожи по свойствам на UHs. Сопровождающееся самораскаливанием металла активное взаимодействие с водородом ( под атмосферным давлением) тория наступает лишь около 500 С. Однако практически такой состав не достигается. [14]
Все актиниды могут быть поглощены на катионитах из слабокислых растворов. При этом чрезвычайно высокое сродство к иони-ту характерно для тория. Так, в солянокислой среде торий удерживается катионитами более прочно, чем другие металлы, и благодаря этому может быть отделен от них с помощью сульфокатионита. [15]
Страницы: 1 2 3 4
