Актиномицин
Cтраница 1
Актиномицины являются мощными ингибиторами ДНК-зависимого синтеза РНК, что применяется в клинике при лечении некоторых видов опухолей. Следует отметить широкий спектр биологического действия депсипептидов - они обладают антибиотической, противоопухолевой, инсек-цидной и др. активностями. [1]
Актиномицины ингиоируют рост грамположительных. [2]
Актиномицины представляют собой желтовато-красные высокотоксичные антибиотики, продуцируемые различными штаммами Streptomyces. Термин актиномицин был предложен Ва-ксманом и Уордрафтом [2408, 2409], - которые еще в 1940 г. выделили актиномицин А из Streptomyces antibioticus. Молекула актиномицинов состоит из хромофора и пептидной части, поэтому природные соединения такого типа часто называют хро-мопептидами. С точки зрения биологической активности актино-мицины характеризуются цитостатическим действием, способностью замедлять развитие опухолей, а также активностью против лимфогранулематоза ( ср. [3]
Актиномицин С содержит треонин, саркозин, пролин, валин, адло-изолейцин и N-метилвалин. По аминокислотному составу указанные антибиотики можно разделить на две группы: 1) А, В и D не содержат одло-изолейцина, 2) С содержит эту аминокислоту. [4]
Актиномицины, обозначения которых приведены в скобках, хроматографически не отличаются от актиномицинов, приводимых перед ними. [5]
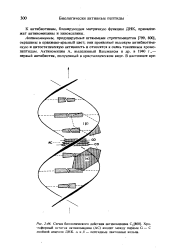 |
Схема биологического действия актиномицина Cj. Хромофорный остаток актиномицина ( АС входит между парами О - С двойной спирали ДНК. а и в - пептидные лактонные кольца. [6] |
Актиномицины, продуцируемые штаммами стрептомицетов [799, 800], окрашены в оранжево-красный цвет; они проявляют высокую антибиотическую и цитостатическую активность и относятся к очень токсичным хромо-пептидам. Актиномицин А, выделенный Ваксманом и др. в 1940 г. - первый антибиотик, полученный в кристаллическом виде. [7]
Актиномицины ингиоируют рост грамположительных. Однако их широкое применение лимитирует высокая токсичность. Для мышей летальная доза актииомицина С составляет 0 5 - 1 мг / кг, доза, переносимая в течение многих дней, - 0 1 мг / кг. [8]
Актиномицины, впервые выделенные в 1940 г. из культуральной жидкости одного из видов Streptomyces ( Actinomyces) группой Ваксма-на, образуются большим числом актиномицетов. Широкий спектр действия актиномицинов, в частности их противоопухолевая активность, определяется способностью образовывать молекулярные ассо-циаты с ядерной ДНК во много раз эффективнее, чем с РНК или доу-гими компонентами клетки: внедряясь между двумя спиралями ДНК они избирательно нарушают способность ДНК служить матрицей для синтеза ядерной РНК и тем самым подавляют в самом зародыше образование всех жизненно важных белков. К числу антибиотиков, действующих на уровне ДНК / РНК, относятся и митомицины, например митомицин А ( 237), выделенный из S. Их мишенью также служит ядерная ДНК, к которой они благодаря наличию в их молекулах нескольких реакционных центров пришиваются ковалентными связями. [9]
Актиномицин С содержит треонин, саркозин, пролин, валин, алло-изолейцин и N-метилвалин. По аминокислотному составу указанные антибиотики можно разделить на две группы: 1) А, В и D не содержат алло-изолойцина, 2) С содержит эту аминокислоту. [10]
Актиномицин D - это антибиотик, выделенный из Streptomyces. Его молекула имеет довольно сложную структуру: она построена из двух коротких пептидных цепей, связанных амидной связью с производным феноксазина. In vivo актиномицин D в низких концентрациях ингибирует синтез РНК, но не ингибирует синтеза ДНК. Было показано, что этот антибиотик прочно связывается с ДНК, но не взаимодействует с РНК. Естественно предположить, что связывание актиномицина D с ДНК препятствует синтезу РНК на ДНК-матрице, но не препятствует синтезу самой ДНК. [11]
Другие актиномицины имеют сходное строение, отличаясь, по-видимому, лишь строением полипептидных цепей. [12]
Актиномицины Ваксмана 96 ] и Брокмапа [13], азосерин Фусарн и другие [34] из Slreptomyces, саркомициы Умезава [91] из Streptomijc. [13]
Актиномицин D тормозит синтез РНК в ин-тактных клетках. [14]
Если актиномицин D вводится через 20 час. Таким образом, и эти результаты полностью совпадают с данными, полученными при облучении регенерирующей печени. Как известно, действие этих антибиотиков направлено на определенные стадии белкового синтеза. Пуромицин нарушает процесс формирования полипептидных цепей на рибосомах, а актиномицин D блокирует синтез иРНК, связываясь с ДНК-матрицей. Поэтому вполне вероятно, что действие ионизирующей радиации может направляться на эти же звенья белкового синтеза. Любопытно, что синтез ДНК в регенерирующей печени блокируется и в том случае, если облучение животных проводится до операции частичной гепатоэктомии. Возможной причиной этого является поражение ДНК-матрицы под действием излучения. [15]
Страницы: 1 2 3 4