J-орбиталь
Cтраница 1
Участие J-орбиталей приводит к трем следствиям. [1]
Пространственное расположение химически связанных атомов определяется направленностью р - и J-орбиталей, а также их гибридизацией с s - орбиталями. [2]
Представления о сильных и слабых полях лигандов, а также данные об относительных энергиях J-орбиталей в полях различной симметрии привлекаются в рамках ТК. С этой целью вводится понятие энергии стабилизации кристаллическим полем ( ЭСК. Необходимо установить электронную конфигурацию центрального иона в сильном или слабом поле лигандов и подсчитать общую энергию электронов. [3]
Помимо рассмотренных примеров гибридизации орбиталей возможны и другие типы гибридизации, в частности, гибридизация с участием J-орбиталей ( см. разд. [4]
Становится также понятным, почему ионы Си бесцветны, тогда как ионы Си2 окрашены: ион Си имеет конфигурацию с / 10, в нем заполнены все / - орбитали, поэтому переходы электронов с одной / - орбитали на другую невозможны, у иона Cu2 ( tf) одна J-орбиталь свободна. [5]
 |
Типы гибридизации и соответствующие им геометрические формы комплексов. [6] |
В комплексе положительный ион-кэмплексообразователь окружен лигандами, которые могут быть или отрицательными ионами, или полярными молекулами, которые обращены к комплексообразователю своим отрицательным концом. Между электронами J-орбиталей иона-комплексообразователя и отрицательными лигандами действуют силы отталкивания, которые увеличивают энергию / - электронов. При этом электростатическое воздействие лигандов на различные J-орбитали неодинаково, так как поле лигандов не обладает сферической симметрией. [7]
 |
Типы гибридизации и соответствующие им геометрические формы комплексов. [8] |
Для образования донорно-акцепторных связей в комплексах могут использоваться не только s - и р-орбитали, но и - орбитали. В этих случаях согласно теории валентных связей происходит гибридизация с участием J-орбиталей. [9]
К сожалению, приходится признать, что хотя к настоящему времени накоплен большой экспериментальный материал по структурам органических производных элементов группы IVs ( главным образом, кремния и олова), теоретическая трактовка полученных результатов нередко оказывается противоречивой. Невыясненным остаются вопросы о роли р л - л-сопряжения и его возможном влиянии на длины связей М - С, об участии J-орбиталей центрального атома в образовании связей при повышении координационного числа, о природе слабых взаимодействий. Решение этих вопросов требует систематических структурных исследований и квантовохимических расчетов, которые в настоящее время для элементоорганических соединений практически отсутствуют. [10]
Как и для элементов IV группы, наблюдается существенное различие между первым элементом группы и остальными. Кроме того, фосфор, мышьяк, сурьма и висмут отличаются от азота тем, что их d - орбитали энергетически доступны; использование J-орбиталей может приводить к увеличению валентности этих элементов до пяти или шести. Конечно, полное включение 3 rf - орбиталей в схему образования о-связей, скажем, РС15, является упрощением, но оно оправдано в рамках этой книги. Читатели, интересующиеся этим вопросом, могут обратиться к недавнему обзору Митчела [14], в котором обсуждается роль rf - орбиталей в образовании связей элементами второго и третьего периодов, и к двум статьям ( Раук и др. [15]; Хофман и др. [16], в которых получены молекулярные орбитали гипотетической молекулы РН5 и обсуждается степень участия Зс. [11]
Таким путем удается объяснить валентность в простейших соединениях. Переменная валентность атомов 3-го периода ( например, хлора и серы) в отличие от постоянной у атомов рассмотренного 2-го периода ( соответственно фтора и кислорода) объясняется в этой теории существованием в третьем квантовом слое вакантных J-орбиталей, которых нет-во втором. [12]
Формулы (7.10) объясняют происхождение символов - орбиталей. Форма граничных поверхностей d - электронных облаков весьма существенна при объяснении химической связи в комплексных соединениях переходных металлов. Угловая составляющая при этом напоминает рассмотренную только что для J-орбиталей. [13]
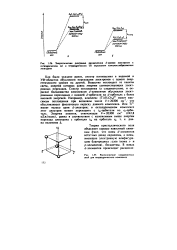 |
Энергетически диаграмма расщепления rf - уровия электронов в октаэдрическом ( а и тетраэдрическом ( б окружении комплексообраэователя лигвндами. [14] |
Как было указано ранее, спектр поглощения в видимой и УФ-областях обусловлен переходами электронов с одного энергетического уровня на другой. Вещество поглощает те кванты света, энергия которых равна энергии соответствующих электронных переходов. Спектр поглощения ( а следовательно, и окраска) большинства комплексов / - элементов обусловлен электронными переходами с низшей / - орбитали на J-орбиталь с более высокой энергией. Ион Ti3 имеет только один / - электрон; в октаэдрическом комплексе этот электрон может переходить с / 2-орбитали на е - орби-таль. [15]
Страницы: 1 2