L-пролин
Cтраница 2
В опытах на крысах испытывали влияние биофлавоноидов - чайных катехинов 100 % - ной чистоты, рутина, кверцетина, геспери-дина, нарингина, эскулина - и некоторых простейших фенолъ-ных соединений - протокатеховой, гомованилиновой кислот и флороглюцина, а также АК - на окисление гомогенатами печени крыс L-пролина и L-оксипролина. В опыт брали белых крыс весом 150 - 200 г, находящихся на обычном рационе вивария. [16]
Гомогенаты печени ( 20 %) готовили на 0 9 % - ном растворе KCI. Большинство фенольных соединений, а также L-пролин и L-окси-пролин растворяли в Рингер-бикарбонатном буфере ( рЦ 7 4)), ка-техинъг и АК растворяли в воде. Плохо раствор амые соединения приготовляли в виде суспензии. [17]
Пролин был синтезирован в 1900 г. Вильштеттером [75] из эфира а, 5-дибромпропилмалоновой кислоты. В 1901 г. Фишер [76] получил L-пролин и DL-пролин из гидролизатов казеина и показал, что второй продукт идентичен синтетическому пролину, который он приготовил из фталимидопропилмалонового эфира. Пролин содержится в коллагене, желатине и других белках. Интересным его свойством является растворимость в спирте. На бумажных хроматограммах пролин дает при обработке нин-гидрином желтую окраску, а при действии изатина - синюю. [18]
Так, рацемические а-аминокислоты были успешно разделены на оптически активные антиподы хроматографией на адсорбенте с химически привитыми группировками L-пролина в присутствии ионов меди. [19]
Раствор 1 30 г миллимоля) карбобензилокси - Ь - лейцил - Ь - аланил - Ь - валил - Ь - фенил-аланилглицина и 0 40 г ( 4 миллимоля) триэтиламина в 25 мл диметилформамида охлаждают до - 5 и при перемешивании прибавляют 0 31 г ( 10 % - ный избыток) изобутилового эфира хлоругольной кислоты. Выдерживают 10 мин при той же температуре, прибавляют раствор 0 48 г ( 2 миллимоля) хлоргидрата бензилового эфира L-пролина в 20 мл диметилформамида и смесь быстро нагревают примерно до 70, после чего сразу же охлаждают. При добавлении избытка воды продукт реакции выпадает в осадок в виде бесцветного твердого вещества. [20]
Для разделения энантиомеров ( оптических изомеров) применяют лигандообменную хроматографию. Так, рацемические а-ами о-кислоты были успешно разделены на оптически активные антиподы хроматографией на хиральном адсорбенте с химически привитыми группировками L-пролина в присутствии ионов меди. [21]
Так, при синтезе грамицидина С из соответствующего пентапептида в качестве промежуточного соединения образуется ассоциат двух молекул пентапептида, причем конформация ассоциата, обусловленная в основном наличием остатков L-пролина и о-фенилала-нина, близка к конформации грамицидина С, что и создает благоприятные условия для удвоения. Важным фактором является, по-видимому, и среднее расстояние между N-концевой аминогруппой и С-концевой карбоксильной группой; это показано, например, изменением конфигурации остатков отдельных аминокислот в вводимом в циклизацию линейном пептиде. Выходы LD-соединения значительно выше, чем выходы LL-CO - единения. Аунг [2003], которые сравнением со стерически однородными соединениями показали, что при циклизации H-Gly - DL - Phe-Gly-OR и H-Gly - DL - Phe-Gly-Gly - DL - Phe-Gly-OR в обоих случаях образуется преимущественно LD-циклогексапептид. [22]
Так, при синтезе грамицидина С из соответствующего пентапептида в качестве промежуточного соединения образуется ассоциат двух молекул пентапептида, причем конформация ассоциата, обусловленная в основном наличием остатков L-пролина и о-фенилала-нина, близка к конформации грамицидина С, что и создает благоприятные условия для удвоения. Важным фактором является, по-видимому, и среднее расстояние между N-концевой аминогруппой и С-концевой карбоксильной группой; это показано, например, изменением конфигурации остатков отдельных аминокислот в вводимом в циклизацию линейном пептиде. Выходы LD-соединения значительно выше, чем выходы LL-соединения. Аунг [2003], которые сравнением со стерически однородными соединениями показали, что при циклизации H-Gly - DL - Phe-Gly-OR и H-Gly - DL - Phe-Gly-Gly - DL - Phe-Gly-OR в обоих случаях образуется преимущественно LD-циклогексапептид. [23]
Из спорыньи ( Claviceps purpurea) выделен целый ряд алкалоидов и частично установлено их строение. При гидролизе таких алкалоидов получены лизергиновая кислота, аммиак и ряд амино - и а-кетокислот, в том числе а-кетоизовалерьяновая кислота, пировиноградная кислота, L-лейцин, L-валин, L-фенилала-иин и L-пролин. [24]
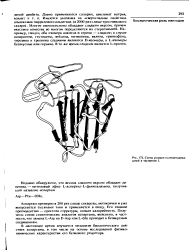 |
Схема укладки полипептидных цепей в тауматине I. [25] |
Многие аминокислоты обладают сладким вкусом, причем вкусовые качества во многом определяются их стереохимией. Например, глицин, оба изомера аланина и серина - сладкие; а случае аспарагина, гистидина, лейцина, метионина, валина, триптофана, тирозина и треонина сладкими являются D-изомеры, а L-изомеры безакусные или горькие. В то же время сладким является L-пролин. [26]
Лизергиновая кислота в спорынье присутствует в форме амидов. Самый простой по структуре эргометрин 6.427 в качестве аминной компоненты содержит пропаноламин. У более сложных, показанных в формуле 6.429, амин-ная часть представлена трициюшческой структурой, возникшей при конденсации L-пролина и двух других аминокислот. [27]
Оба препарата по механизму своего действия ингибируют ангиотензинпревращающий фермент ( см. разд. Полагают, что эналаприл является пролекарством, распадающимся в результате метаболизма с образованием лекарственной молекулы. В настоящее время продолжаются многочисленные синтезы родственных соединений этого класса лекарственных веществ Каптоприл представляет собой 1 - [ ( 25) - 3-меркапто - 2-метилпро-пионил замещенный L-пролин. [28]
Однако методы ГЖХ, как можно полагать, находят применение только в аналитических целях. Колоночная жидкостная хроматография при пониженном давлении представляется более предпочтительной для препаративного варианта, но до сих пор еще ни одна система не применена для разделения аминокислот. Найдено, что оптически активные аминокислоты в виде металлокомплексов являются хорошо разделяющими агентами, хотя испытано лишь несколько субстратов. Присоединение L-пролина к сополимеру хлорметилироваиного стирола с дивинилбензолом с последующей обработкой сульфатом меди приводит к сорбенту, который легко разделяет DL-пролин. Разумеется, использование энантиомера для разделения аминокислот неудобно, однако это не всегда обязательно. [29]
Для накопления этой аминокислоты важным условием является полное или частичное подавление активности а-кетоглутаратдегидрогеназы. Образование продукта увеличивается при добавлении fi - лактамных антибиотиков ( пенициллина, цефалоспорина С), поверхностно-активных веществ и жирных кислот. Влияние двух последних агентов обусловлено увеличением проницаемости клеточных мембран для глутамата, которая зависит от внутриклеточной концентрации жирных кислот и липидов. Путем изменения условий среды процесс ферментации, в ходе которого образуется L-глутамат, может быть переключен на синтез L-глутамина или L-пролина. При высокой концентрации биотина и ионов аммония создаются благоприятные условия для образования L-пролина, а при больших концентрациях аммония и ионов цинка в слабо кислой среде усиливается синтез L-глутамина. DL-аланин, видимо, образуется в реакции трансаминирования при участии пирувата; затем он подвергается рацемизации ферментом аланинрацемазой. [30]
Страницы: 1 2 3