N-окись - пиридин
Cтраница 2
Случай с N-окисью пиридина является еще более наглядным, так как у-положение пиридина - самое реакционноспособное по отношению как к электро-фильным, так и к нуклеофильным реагентам. Поэтому N-окись пиридина очень легко нитруется в у-поло-жении с образованием нитропроизводного, которое с метилатом натрия легко обменивает нитрогруппу на метоксил. [16]
Пример с N-окисью пиридина может быть также объяснен аналогичным образом, поэтому подробно повторять для него рассуждения, нет необходимости. [17]
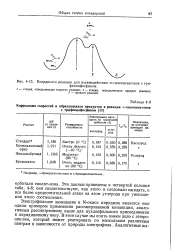 |
Координата реакции для взаимодействия а-галогенкетонов с три. [18] |
Электрофильное замещение в N-окиси пиридина является еще одним примером применения рассматриваемой концепции, аналогичным рассмотренному выше для нуклеофильного присоединения к пиридиниевому иону. В этом случае мы опять имеем дело с гетеро-циклом, который может реагировать по нескольким различным центрам в зависимости от природы электрофила. [19]
Окси - и аминопроизводные N-окиси пиридина также способны к таутомерии. Они были исследованы несколькими физическими методами. [20]
Расчет для раствора N-окиси пиридина в жидком аммиаке приводит к значению умакс 36100 см-1. Разница между экспериментальным и вычисленным значением v3Kcn - vabi4 может свидетельствовать о наличии водородной связи, которая неодинаково стабилизирует основное и возбужденное состояния. [21]
Другие способы получения N-окиси пиридина, в частности действием на пиридин надбензойной [4] или мононадфталевоп [5] кислотой, практического значения не имеют, поскольку молекулярный вес этих надкислот значительно выше, чем у надуксусной, и в то же время значительно более сложным является выделение N-окиси пиридина из реакционной массы. [22]
Полученный уксуснокислый раствор N-окиси пиридина упаривают на кипящей водяной бане в вакууме 20 - 60 мм. Вначале постепенно отгоняется уксусная кислота, которую отдает при термической диссоциации ацетат N-окиси пиридина, затем перегоняется N-окись пиридина. Собирают предгон с температурой кипения до 104 / 1 мм и основную фракцию с температурой кипения 104 - 108 / 1 л-м. [23]
Исследованы [181] масс-спектры N-окисей пиридина и трех изомерных пиколинов. Атом кислорода оказывает существенное влияние на процессы диссоциативного захвата электронов, вызывая как появление новых возбужденных состояний молекулярных отрицательных ионов, так и изменение возможных каналов распада молекулярных ионов. По положению максимумов эффективного выхода ионов на шкале энергии электронов и по направлениям распада были выделены пять основных состояний возбужденных молекулярных ионов, обозначенные буквами а-е. Низкоэнергетическое состояние а представлено в спектре N-окиси пиридина линиями осколочных ионов ( М - Н) -, NC3Hg NC3H, NCs-Относительные интенсивности пиков указанных ионов сравнительно невелики, а максимальная эффективность образования наблюдается при энергии электронов 0 2 - 0 5 эв. [24]
Описан метод экстракции N-окисей пиридина из мочи. [25]
В кипящий раствор N-окиси пиридина в диоксане или воде в течение 3 яас пропускают слабый ток С. [26]
Другие способы получения N-окиси пиридина, в частности действием на пиридин надбензойной [4] или мононадфталевой [5] кислотой, практического значения не имеют, поскольку молекулярный вес этих надкислот значительно выше, чем у над уксусной, и в то же время значительно более сложным является выделение N-окиси пиридина из реакционной массы. [27]
У иона пиридиния и N-окиси пиридина мезомерный эффект вообще не имеет места. [28]
Окиси пиразинов, подобно N-окиси пиридина, можно превратить в га-логенированные основания. [29]
Смесь 0 015 моля N-окиси пиридина и 0 015 моля фенилового эфира р-хлорэтилфосфоновой кислоты нагревают при 80 35 - 40 минут, при 100 2 часа и при 150 6 часов. К полученной реакционной смеси прибавляют раствор едкого натра до - нейтральной реакции, затем смесь разбавляют водой и экстрагируют бензолом. [30]
Страницы: 1 2 3 4