Дихлорэтан
Cтраница 2
Дихлорэтан применяется для депарафинизации в смеси с бензолом в соотношении 78: 22 ( объемн. Недостатками процесса является высокая токсичность дихлорэтана, образование в процессе его регенерации соляной кислоты, разъедающей аппаратуру, и снижение выхода депарафинированного масла по сравнению с выходом при применении смеси метил-этилкетон - бензол - толуол. [16]
Дихлорэтан используется для депарафинизации в смеси с бензолом аналогично тому, как используется ацетон или метилэтилкетон в смеси с толуолом. Соотношение растворителей в смеси зависит от качества исходного дистиллята. [17]
 |
Придципиальная схема процессов депарафинизации масел с применением растворителей. [18] |
Дихлорэтан СаШСЬ используется для депарафинизации в смеси с бензолом. Условия депарафинизации примерно те же, что и для бензол-кетон-толуола. На действующих установках церезин удаляется при помощи центрифуг. [19]
Дихлорэтан при высокой температуре разлагается с образованием ( в присутствии водяного пара) соляной кислоты, поэтому во избежание коррозии растворитель отгоняют в специальных кубах только с закрытым паровым нагревом без впуска открытого пара. [20]
Дихлорэтан - дешевый хороший растворитель для жиров, воска, смол и каучука, обладающий малой летучестью и сравнительно не опасный в пожарном отношении, а также ценный полупродукт в производстве каучука и пластмасс. При работе следует учитывать его большую токсичность. [21]
Дихлорэтан ( С1СН2 - СН2С1) - бесцветная жидкость со сладковатым запахом. [22]
Дихлорэтан ( ГОСТ 1942 - 86) получают хлорированием этилена. Различают два изомера: 1 1 - и 1 2-дихлорэтаны. Первый изомер отличается значительно меньшей токсичностью, второй - вызывает коррозию металла. [23]
Дихлорэтан ( симметричный 1 2-дихлорэтан) - хлористый; этен - относится к классу хлоропроиэводвых углеводородов жирного ряда. [24]
Дихлорэтан является продуктом, находящимся на грани горючих и негорючих органических веществ. Он с трудом воспламеняется и горит коптящим пламенем; пламя дихлорэтана можно легко погасить водой в начальный период горения вследствие его плотности, превышающей плотность воды. Имеются указания, что при интенсивном горении дихлорэтана тушение его аодой может вызвать взрыв образующейся смеси окиси углерода и водорода с воздухом. Дихлорэтан обладает стойкостью к окислению; он термически нестабилен и разлагается при нагреве до 140 с выделением свободного хлористого водорода. При весьма высокой температуре дихлорэтан распадается на хлористый водород и хлористый винил. [25]
Дихлорэтан обладает токсическим действием и является сильным наркотическим средством. При отравлении дихлорэтаном наблюдаются слабость, головокружение, сонливость, головная боль, сладкий вкус во рту, тошнота и позывы на рвоту, легкое раздражение слизистых оболочек и покраснение кожи; в более серьезных случаях, вызванных продолжительным вдыханием дихлорэтана. [26]
Дихлорэтан хлорируется в перхлорэтилен при 300 С в присутствии СиС12 на активированном угле [181] в присутствии смеси А1С13, NaCl и FeCl3 [182] или в кипящем слое при 350 - 450 С на смеси CuCl2, ZnCl2 и CdCl2, нанесенных на целит. Аналогично осуществляется процесс по методу оксихлорирования в присутствии СиС12 - КС1 на отбельной земле. [27]
Дихлорэтан предложен в качестве третьего компонента при перегонке нераздельно кипящих ( азеотропных) смесей; так, например, при перегонке 1водного раствора уксусной кислоты вода отгоняется вместе с дихлорэтаном при температуре ниже точки кипения уксусной кислоты. [28]
Дихлорэтан получают в заводском масштабе, так как он является ценным растворителем и заменителем огнеопасного бензина при экстракции растительных масел. В последнее время дихлорэтан нашел довольно широкое применение для переработки в эфиры гликоля, для получения этилендиамина, дибензила и др. Особый интерес представляет использование дихлорэтана для получения тио-пластов. [29]
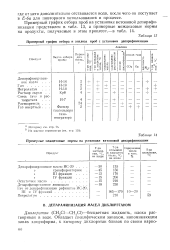 |
Примерный график отбора и анализа проб с установки депарафинизации. [30] |
Страницы: 1 2 3 4