Ара-положение
Cтраница 1
Если же ара-положение блокировано, то реакции может не пройти совсем или же принести к. XI), ца ряду с которым присутствуют только следы 2-окси - 3 Д5 - тримстилбенз-альдегида ( XIII); этот пример свидетельствует о том, что стремление к гсара-замещепию является настолько сильным, что замена алкильной группы на альдегидную протекает предпочтительно перед орто-згметением. В таблицах приведено еще несколько других примеров деа л копирования бензольных производных. [1]
Специфичность га ара-положения в реакциях замещения такого рода зависит в значительной степени от характера применяемого реагента. [2]
Если в ара-положении в бензолсульфокислоте находится электронодонорная группа, например метокси - или метил, то скорость гидролиза значительно ниже; напротив, скорость реакции возрастает, если присутствует электроноакцепторная группа, например нитрогруппа. [4]
Заместители в ара-положении вызывают батохромный сдвиг этой полосы, в го время как орго-заместители - гипсохромный, что вызвано нарушением копланарности фенильных колец. [5]
Наличие в ара-положении нитрозогруппы увеличивает чувствительность к нуклеофильной атаке. [6]
Большая эффективность нитрогруппы в ара-положении объясняется, вероятно, стерическим барьером в компланарности кольца и о-нитрогруппы или групп в комплексе, даже несмотря на то что такой барьер может быть много меньше, чем в обоих исходных ароматических соединениях. [7]
Однако для этого в ара-положении должен быть заместитель ( т рег-бутильиая, октальная или нонильная группа), в противном случае реакция конденсации смолы будет протекать значительно быстрее взаимодействия смолы с каучуком. Используемые для вулканизации смолы с температурой плавления 55 - 65 С, вводимые ( в зависимости от типа каучука и требуемой степени вулканизации) в количествах от 5 до 12 %, состоят в основном из n - октилфенола. Для повышения скорости вулканизации применяют активаторы вулканизации: пнромеллитовый и фталевыи ангидриды или фумаровую кислоту - для бутадиеннитрильного каучука; толуолсульфокислоту или хлор-уксусную кислоту - для бутадиенстирольного каучука; SnCI2 2Н2О или ZnO в смеси с хайпалоном и неопреиом - для бутадиенового каучука. [8]
Замыкание цикла обычно идет в ара-положение к заместителю в бензольном кольце, однако в некоторых случаях получается смесь 5 - и 7-замещенных изохинолинов. Альдегиды с орто - или пара-заместителями и кетоны образуют изохинолины с очень низкими выходами или совсем не вступают в реакцию. [9]
Следует иметь в виду, что ара-положение является сопряженным с атомом углерода карбоксильной группы, а из мета-по-ложения эффект сопряжения заместителя передается только на атомы углерода бензольного ядра. [10]
Заместитель направляется в орто - или ара-положение, как и при других. Незамещенные полициклические ароматические соединения, кроме нафталина, фенантрена и хризена, взаимодействуют с реагентами Вильсмейера, давая с хорошими выходами альдегиды ( табл. 5.3.6), и часто это служит наилучшим методом их синтеза, поскольку Практически эта реакция чрезвычайно проста. Когда она только была открыта, лучшим реагентом считался МФА, а сорастворителем служил о-дихлорбензол. [11]
Третичные олефины легче всего вступают в свободное ара-положение. Если же 3 - е и 5 - е положения в молекуле фенола заняты, то тогда такие фенолы не алкилируются вовсе. Такая дифференцированная реакционноспособность была использована для разделения изомерных замещенных фенолов, температуры кипения которых настолько мало отличаются друг от друга, что и: невозможно разделять ректификацией. При обработке смеси 2 5-диметилфенола и 2 4-диметилфенола, кипящих при одинаковой температуре ( 211 5 С), изобутиленом в количестве, рассчитанном только на алкилирование 2 4-диметилфенола, только последний вступает в реакцию. Это облегчает дальнейшее разделение продуктов ректификацией. [12]
 |
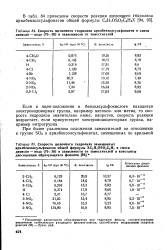
Константы кислотной диссоциации и значения о сульфопроизводных анилина, фенола и бензойной кислоты в 0 1 н. растворе KCI при 25 С. [13] |
Анилины и фенолы, замещенные в ара-положении группой 50з, являются более сильными кислотами, чем соответствующие лега-изомеры. [14]
Наличие двух трудно отщепляемых заместителей в ара-положениях гидразобензола исключает вообще любой вид известных перегруппировок, кроме тех, которые ведут к образованию о-семидииа. Один трудно отщепляемый заместитель в ара-положении исключает образование бензидипа; в этом случае главным продуктом перегруппировки будет дифенилип или о-семидин в зависимости от природы пара-заместителя. Семидины обычно образуются в небольших количествах. Наличие заместителей в гидразобензоле в орто - или лета-положении значительно влияет на направление перегруппировки. Несмотря па необходимость осторожного подхода при интерпретации экспериментальных данных, еще до того, как была понята сложность механизма бензидшговой перегруппировки, из этих данных был сделан вывод, что наиболее важным ориентирующим свойством заместителей является их полярность, как и в большинстве других гетеролитических реакций ароматических соединений. [15]
Страницы: 1 2 3 4