2-метилциклогексанон
Cтраница 1
Радиохимически чистый 2-метилциклогексанон - 1 - С14 получен гидроборированием метилциклогексена. Наряду с синтезированными мечеными стеаратами кобальта и меди ( CoSta - l - C14 и CuSt2 - l - C14 и Go60 ( St) 2) в работе использовались продажные ц-кетоглу-та. [1]
Ан-нелирование 2-метилциклогексанона с метилвинилкетоном, приводящее к ( 73, R Me, R ( D - R ( 4) R ( 9) H)) бшю ИЗуЧено в деталях; в присутствии следов этоксида натрия получали кетол ( 72) ( с выходом до 55 %), который дегидратировали отдельно. [2]
Прямое хлорирование 2-метилциклогексанона приводит к образованию смеси 2 - и 6-хлорпроизводных, но при хлорировании хлористым сульфурилом в четыреххлористом углероде с высоким выходом получается 2-хлоризомер. Отщепление хлористого водорода осуществляют двумя методами. По одному из них неочищенный продукт хлорирования кратковременно нагревают с коллидином при 150 С. [3]
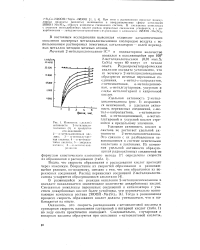 |
Изменение дельты активности 2-метилциклогексанона ( 1 и продуктов. [4] |
Удельная активность 2-метилциклогексанона ( рис. 1) сохраняется неизменной, а удельная активность перекисных соединений, е-ме-тил-к - капролактона, в-кетоэнанто-вой, ы-метиладипиновой, сс-метил-глутаровой и уксусной кислот стремится к предельному значению. [5]
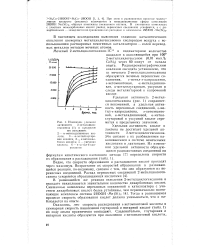 |
Изменение делыюл активности 2-метилциклогексанона ( 1 и продуктов. [6] |
Удельная активность 2-метилциклогексанона ( рис. 1) сохраняется неизменной, а удельная активность перекисных соединений, е-ме-тил-е - капролактона, е-кетоэнанто-вой, u - метиладипиновой, и-метил-глутаровой и уксусной кислот стремится к предельному значению. [7]
Например, из 2-метилциклогексанона с изомерной чистотой более 99 % получается г с-2 - метилцикло-гексанол. [8]
Присоединение метилвинилкетона к 2-метилциклогексанону - 1 с последующей циклизацией путем кротоновой конденсации приводит к окталону ( 461, /) с ангулярной метильной группой. Поскольку присоединение по Михаэлю протекает с большой стереоспецифичностью, оно имеет большое значение для синтезов стероидных соединений. Все известные до сих пор синтезы веществ этого класса проходят через стадию присоединения по Михаэлю. [9]
По аналогии с поведением 2-метилциклогексанона можно ожидать, что при метилировании а-декалона I атаке предпочтительно будет подвергаться атом водорода в положении 9, но прямое алкилирование приводит к образованию в качестве главного продукта 2-метильного производного. Различные косвенные методы алкилирования у Сд включают блокирование 2-метиленовой группы. По одному из методов ( Джонсон, 1947) конденсируют кетон I с этилформиатом и оксиметиленовое производное II превращают в О-изопропильное производное III путем алкилирования йодистым изопропилом. В приведенном случае соединение II образует С-алкильное производное при действии йодистого метила и О-алкильное производное - при действии йодистого изо-пропила. [10]
Таким образом, окисление 2-метилциклогексанона протекает в основном по наименее прочной а - СН-связи. Выход е-кетоэнантовой кислоты в каталитическом и некаталитическом процессах существенно различается и определяется регулирующей ролью комплексов солей переходных металлов, как с исходным 2-метилциклогексаноном, так и с а-кето-гидроперекисями и, вероятно, с радикалами. [11]
Таким образом, окисление 2-метилциклогексанона протекает в основном по наименее прочной а - СН-связи. Выход е-кетоэнактовой кислоты в каталитическом и некаталитическом процессах существенно различается и определяется регулирующей ролью комплексов солей переходных металлов, как с исходным 2-метилциклогексаноном, так и с и-кето-гидроперекисями и, вероятно, с радикалами. [12]
При изучении реакции восстановления 2-метилциклогексанонов посредством RMgX выяснено, что пространственное строение образовавшегося вторичного спирта зависит от строения R: s - C4H9MgBr дает цис-изомер, а i - C4H9MgCl, tf - CgHuMgCl и i - C4H9MgBr дают транс-изомеры. С удалением метальной группы от карбонильной результат реакции меняется, и 3-метил-циклогексанон независимо от пространственного строения R дает только цис-изомер, тогда как 4-метилциклогексанон с теми же восстановителями дает только транс-изомер. [13]
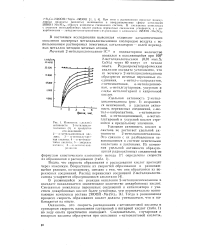 |
Изменение дельты активности 2-метилциклогексанона ( 1 и продуктов. [14] |
В развившейся же реакции окисления 2-метилциклогексанона в оксидате накапливается значительное количество дикарбоновых кислот. Тогда в развившемся процессе скорость образования кислот должна уменьшаться, что и наблюдается на опыте. [15]
Страницы: 1 2 3 4