Фенильное кольцо
Cтраница 3
 |
Константы СТВ ( в мТ некоторых триарилметилов. [31] |
Это вызвано увеличением отклонения фенильных колец от копланарности. [32]
Заместители в - положении фенильного кольца стирола оказывают различное влияние на порядок присоединения диборана. [33]
Полимерный радикал присоединяется к фенильному кольцу. [34]
Джонсон присоединял нитрогруппу к фенильному кольцу в орто - и пара-положениях по отношению к диоксиборилу. [35]
Внедрение метиленовой группы между фенильным кольцом и дисуль-фидным мостиком приводит к тому, что прочность S-S - связи в дибензил-дисульфиде становится такой же, как в алкилдисульфидах. [36]
В них пара-положения в фенильном кольце блокированы, но сопряжение ослаблено. [37]
Во втором соединении одно из фенильных колец трифенилфосфитного лиганда связано ковалентной связью с циклопентадиенильным. [38]
Введение различных заместителей в пара-положение фенильных колец дифенилдисульфида приводит к упрочнению S-S - связи в замещенных дифенилдисульфидах. [39]
Место присоединения полимерного радикала к фенильному кольцу показано условно. [40]
Чем больше электроотрицательность заместителя в фенильном кольце сульфоксидного остатка, тем труднее идет реакция. Действительно, при Дг и - МеСбН4 для завершения реакции требуется 1 час ( 100 С), при Ph, СН2Рпил - МеОС6Н4 - Зчаса ( 110 С), при и - С1С6Н4 - - 6 час. [41]
Чем больше электроотрицателъность заместителя в фенильном кольце сульфоксидного остатка, тем труднее идет реакция. Действительно, при Аг и - МеСбН4 для завершения реакции требуется 1 час ( 100 С), при Ph, СН2РЬил - МеОС6Н4 - Зчаса ( 110 С), при и - С1С6Н4 - - 6 час. [42]
Замена одного из алифатических радикалов на фенильное кольцо снижает растворимость соответствующих ацилатов и тем самым облегчает их очистку, как это можно видеть из следующего примера. [43]
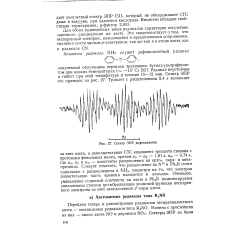 |
Спектр ЭПР дифенилазота. [44] |
СТС компонент триплета связана с протонами фенильных колец, причем а0 ар 1 81 э, ат 0 74 э, где а0, ар и аот - константы расщепления на орто -, пара - и мета-протонах. Следует отметить, что расщепление на N14 в Ph2N почти одинаково с расщеплением в NH2, несмотря на то, что электрон значительную часть времени находится в кольцах. Очевидно, уменьшение спиновой плотности на азоте в Ph2N компенсируется увеличением степени sp - гибридизации волновой функции неспаренного электрона за счет неподеленной 2-пары азота. [45]
Страницы: 1 2 3 4