Установившееся значение - потенциал
Cтраница 2
Предполагая, что скорости электрохимической реакции на хромовом покрытии и массивном хроме различаются мало ( так как диффузионные и кинетические ограничения, а также площадь электрода из-за пор практически не меняются), можно по методу, предложенному в работе [72], определить коррозионный ток элементов, катодом которых является хромовое покрытие, а анодом - сталь 08кп в порах покрытия. Для этой цели на катодной поляризационной кривой массивного хрома ( рис. 44, кривая /) нанесены установившиеся значения потенциалов стали с покрытиями разной толщины. Абсциссы этих точек определяют плотность коррозионного тока. [16]
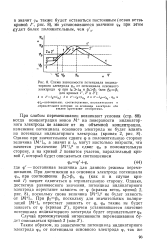 |
Схема зависимости потенциала индика. [17] |
При р2Рь поскольку для значительных поляризаций [ М ] 0 перестает зависеть от ф, фи также не будет зависеть от ф ( кривая 2), причем установившееся значение потенциала индикаторного электрода будет отрицательнее фд. [18]
Легко видеть, что получить экспериментальную кривую abcdf, используя обычный гальваностатический способ, нельзя. Как известно, способ этот характеризуется тем, что между анодом и вспомогательным катодом создается определенная сила тока, после чего измеряется ( по выбранному электроду сравнения) установившееся значение потенциала изучаемого электрода. Такой способ непригоден, так как данному значению тока может отвечать больше чем одно значение потенциала. [19]
Электрохимическую ячейку для снятия кривых объемом не менее 2 л полностью заполняют исследуемой пластовой водой, после чего промывают ячейки 2 - 3-кратным объемом этой воды. СКПК снимают с фиксированием установившихся значений электродного потенциала при различных значениях плотности поляризующего тока. Установившееся значение потенциала определяют измерениями потенциала через каждый час поляризации в первые сутки, а в дальнейшем измерения проводят не реже, чем 2 раза в сутки. Независимо от динамики электродного потенциала в начальной фазе поляризации продолжительность поляризации при каждом значении плотности тока должна составлять не менее двух суток. [20]
На восстановление окислителя расходуются электроны, отбираемые у металла. Смещение потенциала металла продолжается до тех пор, пока скорость его окисления не станет равной скорости восстановления окислителя. Соответствующее установившееся значение потенциала является стационарным потенциалом, при котором и протекает коррозия. [21]
Поскольку в добавляемом растворе перхлората меди отсутствуют ионы одновалентной меди, после введения этой добавки происходит образование и накопление в растворе ионов одновалентной меди. Одновременно потенциалы обоих медных электродов, которые совпадают между собо. В стационарных условиях установившееся значение потенциала является равновесным, так как зависимость установившегося потенциала от концентрации двухвалентной меди подчиняется уравнению Нернста. Следовательно, установившееся значение концентрации одновалентной меди также является равновесным. Этот вывод подтверждается совпадением константы равновесия, рассчитанной из стационарной концентрации одновалентной меди [54], с литературными данными. [22]
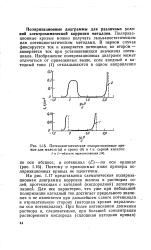 |
Потенциостатические поляризационные кривые для железа ( а и хрома ( б в I н. серной кислоте. / и 2-области перепассивации. [23] |
В первом случае фиксируется ток и измеряется потенциал; во втором - замеряется ток при установившихся значениях потенциала. [24]
В первом случае фиксируется ток и измеряется потенциал; во втором - замеряется ток при установившихся значениях потенциала. [25]
После анодной поляризации индиевого электрода до достижения определенного значении потенциала ток выключали и записывалась кривая спада потенциала до некоторого постоянного значения, затем вновь включался ток анодной поляризации и потенциал доводился до следующего более положительного значения, чем предыдущее. Так как электрод из раствора не извлекался, то последующая анодная поляризация электрода проводится со стационарного состояния, устанавливаемого после выключения поляризующего тока, поэтому последующая анодная поляризация является как бы продолжением предыдущего цикла. Установившееся значение потенциала, по-видимому, определяет стационарное состояние электрода, покрытого окисной пленкой. Путем сопоставления установившихся значений потенциала с потенциалами наиболее вероятных равновесных электрохимических систем можно определить потенциал характерной реакции, которая протекает на электроде в стационарном состоянии, а по виду кривой изменения потенциала во времени - степень устойчивости на электроде. [26]
ЕР, то при MRf окислитель восстанавливается с определенной скоростью. На восстановление окислителя расходуются электроны, отбираемые у металла. Смещение потенциала металла продолжается до тех пор, пока скорость его окисления не станет равной скорости восстановления окислителя. Соответствующее установившееся значение потенциала является стационарным потенциалом, при котором и протекает коррозия. Коррозия металла может быть ускорена одновременным действием нескольких окислителей или контактом металла с другим металлом, имеющим более положительное значение равновесного потенциала. В последнем случае восстановление окислителя протекает за счет электронов, отбираемых от обоих металлов, но скорость коррозии более отрицательного металла возрастает, а скорость коррозии более положительного металла снижается по сравнению со скоростью коррозии этих металлов в отсутствие контакта. [27]
Таким образом, электронный луч заперт. При записи числа сначала на отклоняющие пластины подаются отклоняющие напряжения Ux и Uy, а затем с отставанием в 1 - т - 2 мксек на модулятор М поступает положительный импульс. Тогда электронный луч начинает бомбардировать определенное место экрана. Облучение продолжается несколько микросекунд - этого достаточно для достижения установившегося значения потенциала. [28]
После анодной поляризации индиевого электрода до достижения определенного значении потенциала ток выключали и записывалась кривая спада потенциала до некоторого постоянного значения, затем вновь включался ток анодной поляризации и потенциал доводился до следующего более положительного значения, чем предыдущее. Так как электрод из раствора не извлекался, то последующая анодная поляризация электрода проводится со стационарного состояния, устанавливаемого после выключения поляризующего тока, поэтому последующая анодная поляризация является как бы продолжением предыдущего цикла. Установившееся значение потенциала, по-видимому, определяет стационарное состояние электрода, покрытого окисной пленкой. Путем сопоставления установившихся значений потенциала с потенциалами наиболее вероятных равновесных электрохимических систем можно определить потенциал характерной реакции, которая протекает на электроде в стационарном состоянии, а по виду кривой изменения потенциала во времени - степень устойчивости на электроде. [29]
Основным методом исследования кинетики электрохимических реакций является получение кривых, передающих связь между потенциалом электрода под током и плотностью этого тока. Такие кривые называются обычно t - е - или поляризационными кривыми. Анализ формы поляризационных кривых и изучение характера их зависимости от состава раствора, температуры и других физико-химических параметров позволяют получить довольно полные сведения о природе данного электродного процесса. Поляризационные кривые снимают чаще всего по прямому компенсационному методу. В этом случае на исследуемый электрод подают постоянный ток и измеряют установившееся значение потенциала или, точнее, значение разности потенциалов между исследуемым электродом и соответствующим электродом сравнения. [30]
Страницы: 1 2 3