Изменение - активность
Cтраница 3
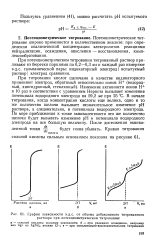 |
График зависимости э.д.с. от объема добавляемого титрованного раствора при потенциометрическом титровании. [31] |
Изменение активности ионов Н в 10 раз в соответствии с уравнением Нернста вызывает изменение потенциала водородного электрода на 59 2 мв при 25 С. В начале титрования, когда концентрация кислоты еще велика, одно и то же количество щелочи вызывает незначительное изменение рН раствора, а следовательно, и потенциала водородного электрода. [32]
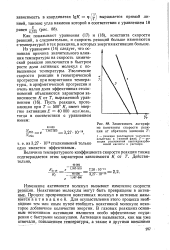 |
Зависимость логарифма константы скорости реак - 327 - Ю-18 ции от обратного значения Т. [33] |
Изменение активности молекул вызывает изменение скорости реакции. Неактивные молекулы могут быть превращены в актив-ные. Процесс превращения неактивных молекул в активные называется активацией. Для осуществления этого процесса необходимо тем или иным путем сообщить неактивной молекуле некоторое добавочное количество энергии. В газовых реакциях основный источником активации являются особо эффективные соударения с быстрыми молекулами. [34]
Изменение активности препарата, содержащего сульфат калия, сопровождается изменением его окраски: ниже 485е - зеленая, в области максимума активности-черная с зеленым оттенком, выше максимума-буровато-красная. Окраска первой по ходу газа части слоя при всех температурах - оранжевая. [35]
Изменение активности препарата, содержащего сульфат калия, сопровождается изменением его окраски: ниже 485 - зеленая, в области максимума активности-черная с зеленым оттенком, выше максимума-буровато-красная. Окраска первой по ходу газа части слоя при всех температурах - оранжевая. [36]
Изменение активности каталазы и пероксидазы под влиянием антнокспдантов отмечено и в эксперименте in vivo. Введение в корм крыс бутилированного гидроксианизола и бутилированного гидро-кситолуола ежедневно в дозах 0 6 и 0 5 г / кг соответственно вызвало в течение 1 - 2 мес. [37]
Изменение активности смеси в требуемое количество раз положено в основу обеспечения регламентированных коэффициентов безопасности по заданному параметру, используемых для оценки уровня взрывозащищенности электрооборудования при его испытаниях. [38]
Изменение активности щелочной фосфатазы в крови и печени указывает на повреждение при дисбалансе аминокислот целостности клеточных мембран, тогда как функциональные сдвиги со стороны кислой фосфатазы, других гидролитических ферментов ( РНК-азы, ДНК-азы, катепсина) и АТФ-азы обнаруживают повреждение в этих условиях лизосомальных и митохонд-риальных мембран. [39]
Изменения спонтанной рекомбинационной активности большей частью специфичны по районам I, II и III хромосомы. [40]
 |
Зависимость ингибирующей активности аценов при окислении церезина при 160 С от концентрации ингибитора. [41] |
Изменение иигибирующей активности аценов может быть вызвано тем обстоятельством. [42]
Изменения двигательной и волевой активности чаще выражаются в двигательной заторможенности, пассивности, испытуемый погружается в свои переживания, исчезают или ослабляются влечения, - сохраняется как бы только констатирующая часть личности. Иногда двигательная заторможенность достигает столь значительной степени, что напоминает катато-нический ступор, на этом фоне могут наблюдаться мутизм и негативизм. Более редко габлюдается упоминавшаяся выше двигательная расторможеиность, подвижность, активность. [43]
Изменение активности КМЦ различных марок в зависимости от величины рН среды может быть объяснена следующим. При значениях рН более 8 0 определяющими являются конформацион-ные факторы, обусловливаемые минерализацией среды, а при высоком содержании щелочных реагентов, кроме того, возможностью течения щелочного гидролиза и других процессов. При значениях рН от 8 0 до 7 0 часть препарата из хорошо растворимой натриевой формы переходит в труднорастворимую водородную форму карбоксиметилцеллюлозы. Этот процесс усиливается при снижении величины рИ среды ниже 7 0, и одновременно возрастает роль кислотного гидролиза, обусловливающего деструкцию макромолекул КМЦ до низкомолекулярных фракций, не обладающих стабилизирующей способностью. С ростом температуры эти процессы значительно интенсифицируются. [44]
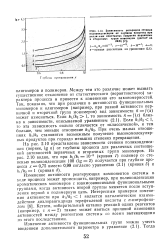 |
Зависимость логарифма степени поликонденсации от глубины процесса при различных константах скорости первичвых н вторичных групп мономеров ( расчет на ЭВМ 17. [45] |
Страницы: 1 2 3 4 5