Выделившийся ион
Cтраница 1
Выделившиеся ионы Mg2 оттитровывают трилоном Б в присутствии хромогена черного. [1]
Выделившиеся ионы Fe ( II) определяют фотометрически с помощью о-фенантролина. [2]
Выделившийся ион никеля определяют титрованием комплексоном в присутствии мурексида в качестве индикатора. Аналогичным образом реагируют любые галогениды серебра. [3]
Выделившиеся ионы никеля определяют титрованием комплек-соном по мурексиду. Так же реагируют все галогениды серебра. [4]
Выделившийся ион Fe ( CN) - понижает окислительно-восстановительный потенциал, и раствор обесцвечивается. [5]
Выделившиеся ионы магния, т.е. заместители кальция, оттитровывают комплексоном III в присутствии хромогена черного. Вычисляют содержание катионов кальция в растворе. [6]
Фотометрический, определение выделившегося иона хлора с роданидом ртути после омыления дихлорэтана, Я. [7]
Тетраэтилсвинец разрушают иодом и определяют выделившийся ион свинца по хромату свинца. [8]
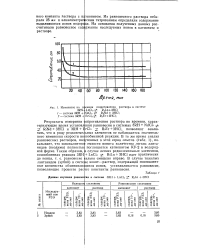 |
Изменение во в 3RH. [9] |
Раствора с к рали 25 мл и алкалиметри выделившихся ионов водор считывали равновесное сод растворе. [10]
Метод основан на разложении ТЭС йодом и определении выделившегося иона свинца с хроматом калия. [11]
Однако конечное значение рН зависит не только от концентрации выделившихся ионов металла, но и от начального рН воды. [12]
Метод основан на разложении ренацита-4 соляной кислотой и колориметрическом определении выделившегося иона цинка с дитизоном. [13]
Метод основан на реакции взаимодействия пестицида с избытком натрия в изопропиловом спирте; выделившиеся ионы хлора определяют титриметрически с нитратом серебра. [14]
При титровании раствором щелочи раствора соли индия, содержащего тартрат или малат, сначала происходит нейтрализация выделившегося иона НзО, а затем - образование растворимых основных оксисоединений индия [346] неустановленного состава. [15]
Страницы: 1 2