Одинаковый ион
Cтраница 1
 |
Теплоты адсорбции СО иг поликристэллических переходных металлах. [1] |
Одинаковые ионы могут различаться строением координационной сферы, что обусловливает появление на поверхности льюисов-ских центров разной силы. Именно такому случаю соответствует рис. 1.3. Приведенный на нем энергетический спектр качественно можно сопоставить с плотностью состояний поверхности ( 100) активного оксида алюминия. Эти состояния формируются гибридными орбиталями алюминия, направленными в сторону недостающего иона кислорода. Общее число состояний в нем меньше, так как ниже концентрация тетраэдрических координированных атомов на поверхности. [2]
 |
Произведения растворимости некоторых солей при 20 С. [3] |
Влияние одинаковых ионов становится весьма существенным для слабо растворимых солей. Ионное произведение не изменяется и в этом случае, однако концентрации отдельных ионов могут значительно меняться в зависимости от наличия в растворе другого источника ионов, одинаковых с одним из ионов соли. [4]
Присутствие в растворе одинаковых ионов оказывает влияние на растворимость всех солей. Кстати, этот способ используется для получения очищенного NaCl. Следует отметить, что применение понятия произведения растворимости к концентрированным растворам неоправданно, поскольку в этом случае нельзя пренебрегать различием между истинными концентрациями ионов в растворе и их активными концентрациями, или активностями. В сильно разбавленных растворах, даже если они насыщенны, активности практически совпадают с концентрациями. [5]
Из-за добавления электролита с одинаковым ионом в растворе увеличивается концентрация ионов К в первом случае и концентрация ионов C1OF во втором, в связи с чем в обоих случаях увеличивается концентрация хлората калия. Поскольку концентрация соли в насыщенном растворе - величина постоянная, то вновь образовавшийся хлорат калия выпадает в осадок. [6]
Так как в ионных решетках одинаковые ионы не могут быть соседями, необходимы какие-либо приближения для определения радиуса ионов. [7]
Исключаем из обеих частей равенства одинаковые ионы. [8]
Если в обеих частях уравнения имеются одинаковые ионы, то их можно не принимать во внимание. Из четырех типов ионов, находящихся в реакционной среде, в обоих случаях реагируют только два - в первой реакции ионы водорода и гидроксильные ионы и во второй ионы водорода и ацетат-ионы. Ионы натрия и хлор-ионы не принимают участия в реакции. [9]
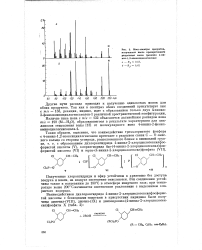 |
Масс-спектры продуктов, полученных после препаративного разделения смеси ( реакция 4-ви-нил - 1, 2 -эпоксициклогексана. [10] |
Другие пути распада приводят к получению одинаковых ионов для обоих продуктов. Так как в спектрах обоих соединений присутствует пик с т / е: 158, реакция, видимо, идет с образованием только двух 4-винил - 2-фениламиноциклогексанолов - 1 различной пространственной конфигурации. [11]
Если при диссоциации электролита образуется несколько одинаковых ионов, то ПР равно произведению активностей ионов в степени, соответствующей количеству образующихся ионов. [12]
Если в состав комплекса вхбдит несколько одинаковых ионов или молекул, то перед названием соответствующего иона или молекулы ставится название соответствующего числа на греческом языке: 1-моно, 2 - ди, 3 - три, 4 - тетра, 5 - пента, 6 - гекса, 7 - гепта, 8 - окто, 9 - нона, 10 - дека, 11-ундека, 12 - додека. [13]
Если два раствора, содержащие различные или одинаковые ионы при различных концентрациях, соприкасаются друг с другом, то на поверхности раздела этих двух сред возникает разность потенциалов. Жидкостные диффузионные потенциалы появляются вследствие того, что разные ионные частицы диффундируют через поверхность раздела фаз с различной скоростью. [14]
Если при диссоциации молекулы электролита образуется несколько одинаковых ионов, то в выражении ПР их концентрации возводятся в соответствующую степень. [15]
Страницы: 1 2 3 4