Ртутный катод
Cтраница 2
 |
Ячейка для электролиза с ртутным катодом. [16] |
Ртутный катод позволяет выделить из раствора много элементов. На ртути велико перенапряжение водорода; при комнатной температуре и плотности тока 0 01 А / см2 оно составляет - 1 04 В. [17]
 |
A. Лабораторный электролизер с ртутным катодом.| Схема лабораторного электролизера с обновляемой поверхностью. [18] |
Ртутный катод 3 толщиной i.2 мм помещается на пористом распределителе потока 4, изготовленном из спеченного стекла. Туда же через трубу 6 поступает азот. Газожидкостная эмульсия проходит в катодное пространство через распределитель 4 и слой ртути, что обеспечивает ее интенсивное перемешивание. [19]
Применение ртутного катода особенно удобно при кулонометрическом методе вследствие тесной связи этого метода с полярографическим методом, в котором также используется ртутный катод. Целесообразно, например, провести качественный полярографический анализ и при помощи полученной полярограммы выбрать подходящие катодные потенциалы для последовательного осаждения различных присутствующих металлов. Обычно бывает достаточно установить в приборе значение потенциала приблизительно на 0 1 или 0 2 в более отрицательное, чем потенциал полуволны осаждаемого иона. [20]
Применение ртутного катода при электролизе растворов хлоридов щелочных металлов вносит в этот процесс ряд существенных особенностей. Вследствие высокого перенапряжения, которое имеется на ртути для выделения водорода, и явлений деполяризации на ртутном катоде разряжаются не ионы водорода, а ионы натрия. [21]
Потенциал ртутного катода незначительно возрастает с повышением концентрации натрия в амальгаме и увеличением плотности тока. [22]
Потенциал ртутного катода в тот момент, когда достигнута величина напряжения разложения и начинается электролиз, называется потенциалом выделения ( или восстановления) данного иона. Потенциал выделения зависит от природы иона, однако на эту величину оказывает влияние концентрация восстанавливающегося иона и некоторые другие факторы. Поэтому для качественного определения ионов пользуются так называемым потенциалом полуволны, который не зависит от концентрации восстанавливающегося иона. [23]
Применение ртутного катода имеет следующие преимущества и особенности в сравнении с платиновым катодом. [24]
Потенциал ртутного катода в тот момент, когда достигнута величина напряжения разложения и начинается электролиз, называется потенциалом выделения ( или восстановления) данного иона. Потенциал выделения зависит от природы иона, однако на эту величину оказывает влияние концентрация восстанавливающегося иона и некоторые другие факторы. Потенциал полуволны не зависит от концентрации восстанавливающегося иона. [25]
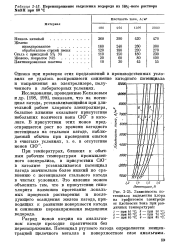 |
Перенапряжение выделения водорода из 16 % - ного раствора NaOH при 80 С.| Зависимость потенциала выделения хлора на графитовом электроде от плотности тока при различных температурах. [26] |
Потенциал ртутного катода определяется концентрацией щелочного металла в поверхностном слое амальгамы. [27]
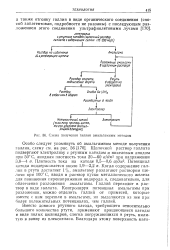 |
Схема получения галлия амальгамным методом. [28] |
Вместо донного ртутного катода, требующего относительно большого количества ртути, применяют вращающиеся катоды в виде полых цилиндров, слегка погружающихся в ртуть, налитую в ванну из плексигласа. [29]
Ширина ртутного катода хлорного электролизера равна 725 мм, длина 7 83 м, толщина 4 0 мм. [30]
Страницы: 1 2 3 4