Основная конфигурация
Cтраница 4
Для решения задач второго комплекса в институте ШИИСДТ-нефть разработаны алгоритмы [ l ] и пакет программ на алгоритмическом языке PL / 1 в среде дОС КС версии 2 Ъ с ориентацией на ЭШ EC-I022 основной конфигурации. Программы написаны применительно к трубопроводной системе, содержащей до 50 РЛ и до 99 ХУ. Время решения задачи зависит от типа используемой ЭВМ, размеров трубопроводной системы и близости начального приближения к искомому решению. [46]
Системы обработки данных ( вычислительные системы) включают в себя центральные процессоры и основные периферийные устройства ( например, устройства накопления и хранения данных, терминалы и др.) наряду с компонентами, добавляемыми к основной конфигурации при создании новой системы. [47]
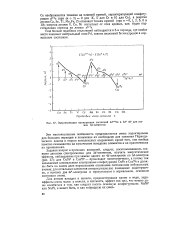 |
Энергетическая конкуренция состояний 3d 14s и 3d 4 г для атомов З - элементов. [48] |
Для атомов ванадия и никеля, предшествующих хрому и меди, эндо-эффекты очень малы: у никеля, в частности, эффект так мал, что можно даже колебаться в том, как следует писать основную конфигурацию: Nid8sa или Nid9s, а может быть, и как гибридную их смесь. [49]
Если предположить, что между оставшимся / - электроном аниона и й2 - электроном взаимодействие является аитиферромапшт-ным, то результирующее эффективное взаимодействие ( косвенное обменное взаимодействие) между ионами М и Мг будет антиферромагнитным или ферромагнитным в зависимости от того, занята орбита d t основной конфигурации А электроном ( если, например, d [ dx) или свободна. [50]
В строгой теории атомов и ионов доказано ( Рид, Саймон, 1982), что при учете кулоновского взаимодействия спектр гамильтониана ( 1) изолированного иона с зарядом Z Z - Ni состоит из дискретной части ( происходящей из одноэлектронных возбуждений, когда возбуждается внешний электрон основной конфигурации) и непрерывной части, соответствующей ионизации. При этом состояния, описываемые возбужденными конфигурациями, с энергией ( 21) в непрерывном спектре, являются долгоживущими квазистационарными. Это подтверждает допустимость описания возбужденных состояний ионов квантовыми числами электронных конфигураций с оценкой времени жизни золотым правилом Ферми. При учете межэлектронного взаимодействия в представлении чисел заполнения на кулоновских волновых функциях многоэлектронный гамильтониан не является диагональным, но недиагональные элементы, связанные с взаимодействием конфигураций, остаются относительно небольшими. Поэтому конфигурационное представление с оболочечной структурой ионов является основным в теории атомов и ионов. Такая ситуация реализуется, вообще говоря, в случае ионов с большими Z и малым числом связанных электронов. [51]
Для конфигурации d2 возможны термы S, D, 1G, 3P, F. Основная конфигурация ( р2) имеет термы - Д Р, S. [52]
Основные конфигурации, содержащие / - оптические электроны, имеют в шестом периоде лантаниды Се, Рг, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tu, Yb, и в седьмом периоде актиниды Ac, Th, Pa, U, Np, Pu, Am, Cm, Bk, Cf. Хотя основные конфигурации лантана ( 5d6s2) и актиния ( 6d 7s2) и не содержат / - электронов, эти элементы принято рассматривать вместе с остальными редкоземельными элементами. [53]
Во второй колонке приведены результаты учета возмущения, обусловленного частью электронного отталкивания, не обладающей сферической симметрией. Основная конфигурация расщепляется на три так называемых терма, а возбужденная конфигурация - на два терма. Этим термам приписывают спектроскопические обозначения, указывающие полный орбитальный угло вой момент и полный спиновый угловой момент электронов. [54]
Во второй колонке приведены результаты учета возмущения, обусловленного частью электронного отталкивания, не обладающей сферической симметрией. Основная конфигурация расщепляется на три так называемых терма, а возбужденная конфигурация - на два терма. Этим термам приписывают спектроскопические обозначения, указывающие полный орбитальный угловой момент и полный спиновый угловой момент электронов. [55]
Для конфигурации d2 возможны термы S, D, 1G, 3P, F. Основная конфигурация ( р2) имеет термы - Д Р, S. [56]
Рассмотрим теперь молекулу азота. Основная конфигурация атома азота есть ( Is) 2 ( 2s) 2 ( 2p) 3, основное состояние - S, и на каждой из трех р-орбиталей находится по одному электрону. Отсюда следует, что каждый из этих трех электронов может образовать связь с соответствующим электроном другого атома: электроны, занимающие Pz-орбитали, образуют а-связь, а электроны, находящиеся на рх - и ру-орбиталях, - две я-связи. Это описание ничуть не хуже того, которое дается методом МО, однако волновая функция, характеризующая эти связи, оказывается довольно сложной. [57]
Страницы: 1 2 3 4