Концентрация - перекись - водород
Cтраница 4
Скорость полимеризации вишлпирролидона резко возрастает увеличением концентрации перекиси водорода и пропорциональ-а корню квадратному из концентрации аммиака. [46]
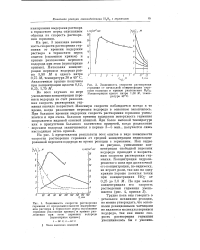
Во всех случаях по мере уменьшения концентрации перекиси водорода за счет разложения скорость растворения германия вначале возрастает. Максимум скорости наблюдается всегда в то время, когда разложение перекиси водорода в основном закончилось. При большем времени выдержки скорость растворения германия уменьшается и при очень большом времени выдержки поверхность германия покрывается видимой окисной пленкой. При более высокой температуре или в присутствии большого количества примесей, когда разложение перекиси водорода заканчивается в первые 3 - 5 мин. [48]
 |
Температуры кипения растворов перекиси водорода при атмосферном давлении. [49] |
Повышение температуры кипения, вызываемое ростом концентрации перекиси водорода, составляет около 1 на 0 02 мольной доли. Точность данных для температур кипения не настолько велика, чтобы можно было пользоваться ими для определения концентрации, если требуется точность, превышающая 0 1 - 0 3 вес. Кроме того, при любых концентрациях вследствие разложения всегда происходит большее или меньшее выделение кислорода, причем температура кипения снижается на величину, соответствующую влиянию парциального давления кислорода над растворами. [50]
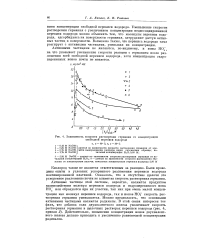 |
Зависимость скорости растворения германия от концентрации свободной перекиси водорода. [51] |
Уменьшение скорости растворения германия с увеличением концентрации недиссоциированной перекиси водорода можно объяснить тем, что молекулы перекиси водорода, адсорбируясь на поверхности германия, затрудняют доступ активных частиц к поверхности. Возможно также, что перекись водорода сама реагирует с активными частицами, уменьшая их концентрацию. [52]
Выход привитого сополимера совершенно явно зависел от концентрации перекиси водорода. [53]
На скорость деструкции полисахарида существенное влияние оказывает концентрация перекиси водорода. Небольшое количество пероксида водорода ( соотношение количества элементарных звеньев хитозана к Н2О2 равно 2: 1) за 30 минут приводит к снижению кинематической вязкости уксуснокислых растворов деструктированного хитозана в 2 раза. Дальнейшее повышение концентрации Н2О2 ( выше 6.0 - 10Н М) не оказывает влияния на снижение молекулярной массы полисахарида. Скорость деструкции существенно возрастает при повышении температуры реакции. Элементный состав хитозана до и после деструкции практически не меняется, но наблюдается некоторое снижение содержания аминогрупп. [54]
Страницы: 1 2 3 4