Атом - цинк
Cтраница 2
Спектры атомов цинка, кадмия и ртути сходны между собой. Зависимость энергии от квантового числа / при данных L и S определяет значение триплетного расщепления: для больших атомных номеров расщепление имеет большее значение. [16]
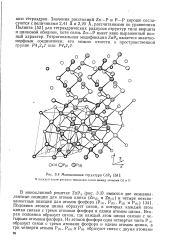 |
Моноклинная структура CdP4. [17] |
Половина атомов цинка образует связи, в которых каждый атом цинка связан с тремя атомами фосфора и одним атомом цинка. Вторая половина образует связи, где каждый атом цинка связан с четырьмя атомами фосфора. [18]
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, d - подуровень второго снаружи электронного слоя целиком заполнен. [19]
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, rf - подуровень второго снаружи электронного слоя целиком заполнен. Однако у элементов подгруппы цинка этот подуровень уже вполне стабилен и удаление из него электронов требует очень большой затраты энергии. Ртуть, кроме того, образует соединения, в которых ее степень окис-ленности равна - f - 1; но, как будет показано ниже ( см. § 216), и в этих соединениях ртуть следует считать двухвалентной. [20]
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, d - подуровень второго снаружи электронного слоя целиком заполнен. [21]
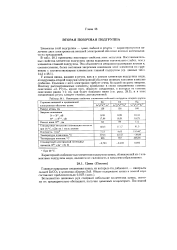 |
Некоторые свойства элементов побочной подгруппы второй группы. [22] |
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, d - подуровень второй снаружи электронной оболочки целиком заполнен и вполне стабилен. Удаление с него электронов требует очень большой затраты энергии. Ртуть, кроме того, образует соединения, в которых ее степень окисления равна 1; но, как будет показано ниже ( см. разд. [23]
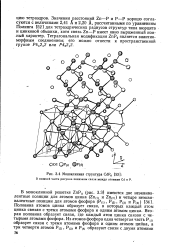 |
Моноклинная структура CdP4. [24] |
Половина атомов цинка образует связи, в которых каждый атом цинка связан с тремя атомами фосфора и одним атомом цинка. Вторая половина образует связи, где каждый атом цинка связан с четырьмя атомами фосфора. [25]
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, d - подуровень второго снаружи электронного слоя целиком заполнен. [26]
Спектры атомов цинка, кадмия и ртути сходны между собой. Зависимость энергии от квантового числа / при данных L и S определяет значение триплетного расщепления: для больших атомных номеров расщепление имеет большее значение. [27]
Например, атомы цинка соединяются с двумя ( не больше и не меньше) органическими группами. [28]
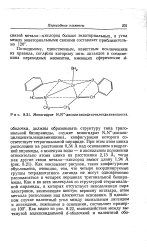 |
Моногидрат К М - дисалицилиденэтиленаиаминцинка. [29] |
При этом атом цинка расположен на расстоянии 0 34 А над основанием квадратной пирамиды, а молекула воды - в аксиальном положении относительно атома цинка на расстоянии 2 13 А, тогда как другие связи металл-кислород имеют длину 1 94 А ( рие. Как показывает рисунок, такая конфигурация обусловлена, очевидно, тем, что четыре координируемые группы тетрадентатного лиганда не могут одновременно располагаться в четырех вершинах тригональной бипирамиды. Как и во всех молекулах со структурой тетрагональной пирамиды, в которых отсутствует неподеленная пара электронов, занимающая шестую вершину октаэдра, атом металла расположен над плоскостью основания. [30]
Страницы: 1 2 3 4