Молекула - большинство - вещество
Cтраница 2
Отдельного рассмотрения заслуживает пока еще мало изученный вопрос о связи между каталитическим действием активных углей и их пористой структурой, поскольку основная часть сорбционного объема обычных образцов углей принадлежит микропорам [2], трудно или даже вовсе недоступным для молекул большинства веществ, подвергающихся каталитическим превращениям. Поэтому в литературе высказывалось мнение [1, 3], что каталитические превращения веществ происходят не на всей, а лишь па очень небольшой - порядка нескольких процентов - части обширной поверхности угля. Было, в частности, найдено [3], что каталитическое окисление сероводорода кислородом воздуха фактически осуществляется только в тех порах угля, диаметр которых лежит в пределах величин 3 5 ч - 8 0 нм. [16]
 |
При сжатии воздуха молекулы его располагаются плотнее. [17] |
Одна из очень крупных молекул - молекула крахмала - имеет размер 5 миллимикронов, молекула воды - около 0 3 миллимикрона. Величина молекул большинства веществ измеряется также десятыми долями миллимикрона. [18]
Парамагнетизм нельзя понять, исходя только из чисто классических соображений, так как основной вклад в парамагнитный эффект вносит магнитный спиновый момент электронов. В атомах и молекулах большинства веществ спиновые магнитные моменты взаимно компенсируются и в целом молекулы немагнитные. Такие вещества являются диамагнетиками. [19]
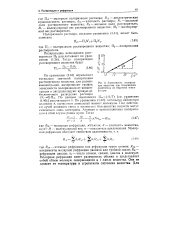 |
Зависимость поляризации вещества при бесконечном разведении от обратной температуры. [20] |
По уравнению (1.42), используя найденную величину Ь, вычисляют дипольный момент молекулы. Под действием лучей видимого света в молекулах большинства веществ могут смещаться лишь электроны. Атомная и ориентационная поляризации в этом случае равны нулю. [21]
Мы рассмотрим слабые вандерваальсовы силы, которые вызывают конденсацию паров, состоящих из молекул с ковалентными связями. Образование ионной решетки является результатом более сильного взаимодействия между молекулами с ионными связями. Но молекулы большинства веществ представляют собой нечто среднее между двумя этими предельными случаями. Очень часто атомы в молекулах удерживаются друг около друга с помощью связей, которые в основном ковалентные, но у которых имеется достаточное разделение зарядов для того, чтобы влиять на свойства молекул. Такие молекулы мы называем полярными молекулами. [22]
В основе эмиссионного спектрального анализа лежит изучение строения света, разложенного по длинам волн в виде спектра, который излучается или поглощается возбужденными атомами и молекулами анализируемого вещества. Атомы и молекулы могут возбуждаться пламенем горелки, электрической дугой или искрой. Высокая температура ( 1000 С) в источниках света приводит к распаду молекул большинства веществ на атомы. Поэтому эмиссионный метод, как правило, является атомным анализом. [23]
Лишь сравнительно недавно многочисленные лаборатории начали проводить широкие исследования проблем генерации плазмы и преимуществ плазмохимических процессов, хотя плазма и ранее находила ограниченное применение для проведения в ней химических реакций, таких, как фиксация азота и синтез ацетилена. На рис. II 1.1 представлена диаграмма состояний веществ при высоких температурах, на основании которой можно сформулировать несколько важных для высокотемпературной химии положений. К нет молекул и могут существовать атомы только некоторых элементов, так как атомы и молекулы большинства веществ при этих температурах ионизированы. Таким образом, термин плазмохимия неудачен, поскольку при плазменных температурах нет молекул веществ. Но мы будем употреблять термин плазмохимия, понимая под ним химию, использующую высокие температуры и высокие энергии плазмы для реакций, проводимых при пониженных по сравнению с плазменными температурах, а также в тех случаях, когда большие скорости теплопередачи, достижимые в плазме, обычно вызывают изменение физических и химических свойств веществ. Графики температурной зависимости энтальпий некоторых одно - и двухатомных газов ( для равновесных условий при 1 атм) приведены на рис. III.2. Для диссоциации двухатомных молекул, происходящей в интервале температур от 4000 до 10 000 К, требуется от 90 до 200 ккал / моль, в то время как для ионизации, протекающей между 10000 и 30000 К, необходимо от 340 до 600 ккал. Максимальные температуры пламен достигают значений - 3000 К, при которых начинается процесс диссоциации молекул; в то же время минимальные температуры плазмы / - 10000 K, так как только при таких температурах достигается степень ионизации, достаточная для протекания тока, необходимого для поддержания плазмы. [24]
Лондоновские силы возникают между любой парой атомов или молекул. Они являются единственными сила: ми, действующими в благородных газах. Пз остальных веществ лишь очень немногие имеют настолько же низкие температуры плавления и кипения, откуда следует, что между атомами и молекулами большинства веществ должны действовать еще и другие, значительно большие силы. Однако лондоновокие силы определяются полной величиной поверхности молекул и могут обусловливать температуры плавления и кипения, которые заметно превышают комнатную температуру. Хорошими примерами в этом отношении являются парафин, а также полиэтилен. [25]
Страницы: 1 2