Нагрев - цеолит
Cтраница 1
Нагрев цеолита до 800 С существенно не изменяет структуру кристаллической решетки; потеря адсорбированной воды происходит при температуре около 200 С, и при этой же температуре отмечено начало выделения аммиака, продолжавшееся до 300 - 350 С. Масса образца в интервале 350 - 500 С не изменилась, однако при дальнейшем повышении температуры начала уменьшать ся; катализатор при этом заметно поглощал тепло. При добавлении воды к цеолиту, предварительно прокаленному до 520 С, гидроксильные группы, по-видимому, образуют водородные связи с молекулами воды. Некоторым подтверждением этого служит то, что после удаления воды в глубоком вакууме в ИК-спектре вновь появились полосы, соответствующие гидроксильным группам. [1]
 |
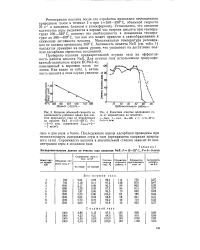
Результаты очистки изопентана от сернистых соединений. [2] |
Из приведенных данных следует, что к применению нагрева цеолитов при их контакте с непредельными углеводородами следует подходить весьма осторожно. Процесс десорбции, видимо, целесообразнее проводить в токе инертных веществ при возможно более низкой температуре. [3]
Каждая - обработка цеолита важна для восстановления структуры, количества и качества активных центров. При нагреве цеолита типа HY выше 500 С он теряет гидроксидные группы, связанные с атомами алюминия. [4]
По результатам исследований статики и динамики адсорбции составлены эмпирические уравнения для расчета исходной адсорбционной емкости цеолита СаА по СО ( расчет по термическому уравнению ТОЗМ дает значительные расхождения с экспериментальными изотермами), динамической активности, степени отработки равновесной емкости и длительности адсорбции. Разработана также методика расчета нагрева цеолита, что позволяет рассчитать полный адсорбционный цикл. [5]
Установлено, что основное количество серы выделяется в первый час нагрева цеолита при температурах 100 - 320 С, поэтому нет необходимости в повышении температуры до 380 - 400 С, так как это может привести к сажеобразованию и снижению активности цеолита. Максимальная температура регенерации не должна превышать 350 С. Активность цеолита NaX ( см. табл. 1) находится примерно на одном уровне, что указывает на достаточно полную десорбцию сернистых соединений. [7]
Структура цеолитов характеризуется наличием большого числа полостей, соединенных между собой окнами, или микроканалами, размеры которых сравнимы с размерами реагирующих молекул. Например, в цеолите типа шабазит имеется 3 - 1020 полостей диаметром 11 4А, в каждую полость которого может вместиться 24 молекулы воды. При нагреве цеолита вода удаляется, и образуется ячеистая структура. Удельная поверхность цеолитов достигает 700 - 1000 м2 / г. Обезвоженные цеолиты способны избирательно адсорбировать молекулы различных веществ в зависимости от размеров каналов. [8]
Наиболее ценными свойствами обладают трехмерные цеолиты, полимерные тела, структура которых подобна структуре полевых шпатов. Большие полости и каналы, ведущие на поверхность кристалла ( окна), имеют строго определенные размеры и в обычном состоянии заполнены молекулами воды и катионами металлов. При нагреве трехмерных цеолитов в вакууме они теряют воду, их внутренние полости освобождаются и могут быть заняты другими молекулами, размеры которых позволят им пройти через окна. Жесткие алюмосиликатные решетки не изменяются при удалении воды из цеолита, и это дает возможность получать пористые кристаллы сорбента со строго определенными размерами окон. Сорбируемые молекулы, особенно полярные, удерживаются в пустотах кристалла силами Ван-дер - Ваальса или электростатическим взаимодействием с функциональными группами алюмосиликатов. [9]
В настоящее время насчитывается несколько десятков разно - вредностей природных и синтетических цеолитов, отличающихся структурой, типом катионов Me, силикатным модулем и числом молекул кристаллизационной воды. Структура цеолитов характеризуется наличием большого числа полостей, соединенных между собой окнами, или микроканалами, размеры которых сравнимы с размерами реагирующих молекул. Например, в цеолите типа шабазит имеется 3 - Ю20 полостей диаметром 11 4 А, в каждую полость которого может вместиться 24 молекулы воды. Диаметр окон шабазита составляет 4 9 А. При нагреве цеолита вода удаляется, и образуется ячеистая структура. Удельная поверхность цеолитов достигает 700 - 1000 м2 / г. Обезвоженные цеолиты способны избирательно адсорбировать молекулы различных веществ в зависимости от размеров каналов. Так, при диаметре канала ( окна) 4 К цеолит не может адсорбировать углеводородов нормального строения, диаметр молекул которых равен 4 9 К. [10]
В настоящее время насчитывается несколько десятков разновидностей природных и синтетических цеолитов, отличающихся структурой, типом катионов Me, силикатным модулем и числом молекул кристаллизационной воды. Структура цеолитов характеризуется наличием большого числа полостей, соединенных между собой окнами, или микроканалами, размеры которых сравнимы с размерами реагирующих молекул. Например, в цеолите типа шабазит имеется 3 1020 полостей диаметром 11 4 А, в каждую полость которого может вместиться 24 молекулы воды. Диаметр окон шабазита составляет 4 9 А. При нагреве цеолита вода удаляется и образуется ячеистая структура. Удельная поверхность цеолитов достигает 700 - 1000 м2 / г. Обезвоженные цеолиты способны избирательно адсорбировать молекулы различных веществ в зависимости от размеров каналов. [11]
В настоящее время насчитывается несколько десятков разновидностей природных и синтетических цеолитов, отличающихся структурой, типом катионов Me, силикатным модулем и числом молекул кристаллизационной воды. Структура цеолитов характеризуется наличием большого числа полостей, соединенных между собой окнами, или микроканалами, размеры которых сравнимы с размерами реагирующих молекул. Например, в цеолите типа шабазит имеется 3 1020 полостей диаметром 11 4 А, в каждую полость которого может поместиться 24 молекулы воды. Диаметр окон шабазита составляет 4 9 А. При нагреве цеолита вода удаляется и образуется ячеистая структура. Обезвоженные цеолиты способны избирательно адсорбировать молекулы различных веществ в зависимости от размеров каналов. Так, при диаметре канала ( окна) 4 А цеолит не может адсорбировать углеводороды нормального строения, диаметр молекул которых равен 4 9 А. [12]
Подобные материалы считаются ультрастабильными. Известно, что ультрастабильные структуры характеризуются уменьшенными на 1 - 1 5 % размерами единичной ячейки и это уменьшение обусловлено удалением атомов алюминия из кристаллической решетки и возможностью их участия в качестве катионов в ионном обмене. Наибольший эффект получается при удалении 30 % алюминия. Каждая обработка цеолита важна для восстановления структуры, количества и качества активных центров. При нагреве цеолита типа HY выше 500 С он теряет гидроксильные группы, связанные с атомами алюминия. [13]
Катализатор прокаливают при высокой температуре, при этом удаляется аммиак, а оставшийся протон занимает место исходного иона натрия. Свойства получаемого в итоге катализатора сильно зависят от условий актива-ционной стадии: температуры и продолжительности активации. Активность катализаторов HY зависит в некоторой степени от способа приготовления. Прокаливание в присутствии NH3 или водяного пара позволяет получить ультрастабильные цеолиты. Как и у аморфных АСК, при нагреве цеолитов выше 400 С уменьшается число центров Бренстеда и возрастает число центров Льюиса. При температуре 1000 С остаются только центры Льюиса. Найдено, что число центров Бренстеда и удвоенное число центров Льюиса постоянны по всем указанным диапазонам температур. Если конечная температура прокаливания не превышает 700 С, то при добавлении воды большинство кислотных центров Льюиса можно вновь превратить в центры Бренстеда. [14]
Повышение температуры слоя при регенерации увеличивает скорость десорбции двуокиси углерода как в случае вакуумирования, так и в случае применения отдувочного газа. На основании анализа опытных данных нами установлено, что при вакуум-термической регенерации для цеолитов типа NaX оптимальной температурой, обеспечивающей полную десорбцию двуокиси углерода при достаточной скорости ее ( при времени, не превосходящем цикла адсорбции и охлаждения), является температура 65 - 80 С. Для цеолитов типа СаА эта температура несколько выше и составляет 100 - 120 С. Такой же порядок температур регенерации остается и в случае применения сухого и свободного от двуокиси углерода продувочного газа. Здесь могут применяться два способа нагрева адсорбента. Первый, когда подвод тепла осуществляется через стенки адсорбера, на практике применяется редко, так как в промышленных условиях диаметр адсорбера довольно большой, а Цеолиты обладают низкой теплопроводностью; второй, когда подвод тепла осуществляется с помощью продувочного газа, нагретого до определенной температуры, применяется чаще. В промышленных условиях довольно редко-имеется в достаточном количестве сухой ( точка росы порядка - 60 С) и не содержащий двуокиси углерода газ. Наиболее часто для целей регенерации используют природный газ или атмосферный воздух. Влажность воздуха меняется в более широких пределах, чему природного газа. В этом случае для удаления двуокиси углерода из цеолитов типа NaX температуру в период десорбции следует иметь 100 - 120 С, а для цеолита СаА - 150 - 180 С. Однако, поскольку требуется удаление не только двуокиси углерода, но и паров воды, температура регенерации должна быть выше. В процессе получения защитных атмосфер, если влажность отдувочного газа составляет 5 - 7 г / м3, нагрев цеолита СаА должен быть проведен до 230 - 250 С. [15]
Страницы: 1