Сернистое железо
Cтраница 3
Сколько сернистого железа необходимо для получения сероводорода при взаимодействии с 20 мл кислоты: а) соляной 21 92 % - ной концентрации; б) соляной пл. [31]
Почему сернистое железо FeS, молекула которого состоит из атомов двух элементов, не является окислом. [32]
Образование сернистого железа из серы и железа является примером реакции соединения. [33]
Образование сернистого железа из порошков железа и серы имеет место и при растирании их под водой / При этом выход продукта реакции даже несколько больше, чем при растирании в сухом виде. Кажется фантастическим предположение, что при растирании под водой также возникают локальные температуры в несколько тысяч градусов, которые должны вызывать реакцию. [34]
Хлопья сернистого железа при отстаивании воды могут оседать на дно либо всплывать в зависимости от агрегации их с пузырьками лаза и. [35]
Осадок сернистого железа ( FeS) получается путем осажде-ния сернокислого железа сульфидом натрия в эквимолярных растворах. Пробирки поверх ватной пробки затыкаются корко-вой. [36]
Осадок сернистого железа отфильтровывают и промывают водой, насыщенной сероводородом. Полученный раствор нейтрализуют серной кислотой до явно кислой реакции и пропускают ток сероводорода в течение 10 - 15 мин. [37]
Осадок сернистого железа будет выпадать лишь при добавлении в раствор сернистого аммония, так как FeS растворим в кислотах. [38]
Образование сернистого железа и диффузия водорода в решетку - два параллельных процесса, обычно происходящих при коррозии железа в водных растворах сероводорода, причем образование сернистого железа не является причиной хрупкости металла. Последняя вызвана исключительно проникновением водорода в металл, что между прочим подтверждает временный характер хрупкости, исчезающей после дегазации. [39]
В сернистом железе 36 4, а в полусернистой меди 20 % серы. [40]
В химически чистом сернистом железе FeS2 содержится 53 46 % S в 46 54 % Fe. Однако в природе в совершенно чистом виде сернистое железо не встречается. В природном колчедане содержание серы составляет 25 - 52 %, а железа 35 - 44 %; остальное приходится на примеси, из которых основными являются сернистые соединения меди, цинка, свинца, мышьяка, никеля, селена, кобальта, теллура, углекислые и сернокислые соли кальция и магния, тальк, кварц часто в незначительных количествах золото и серебро. [41]
При этом сернистое железо служит катодом, а чистая поверхность металла - разрушающимся анодом. Свободный углекислый газ, снижая рН среды, препятствует образованию прочной пленки окислов на поверхности металла. В присутствии СО 2 пленка окислов становится рыхлой и легко смывается потоком жидкости. [42]
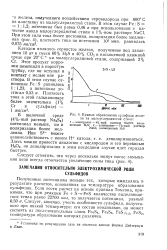 |
Кривые образования сульфида железа на малоуглеродистой стали. / - электролит - 4 % - ный раствор NaOH, насыщенный HzS. 2 - электролит - 1 % - ный раствор NaCi, насыщенный H2S. [43] |
Катодом являлось сернистое железо, полученное под давлением 10 ат в смеси 60 % H2S и 40 % СО2 в насыщенной влажной среде при 20 С на малоуглеродистой стали, содержащей 2 % Сг. [44]
Чем отличается сернистое железо от смеси серы и железа. [45]
Страницы: 1 2 3 4