Объем - прибавленный раствор
Cтраница 2
Титрование ведут обычным способом, перемешивая раствор при ( помощи мешалки. Записывают объем прибавленного раствора кислоты и регистрируют яри этом силу фототока гальванометром. Пока щелочь ие будет вся нейтрализована, титруемый раствор окрашен в желтый цвет. Так как синие лучи сильно поглощаются желтым раствором, то гальванометр будет регистрировать слабые фотатоки, но как только эквивалентная точка достигнута, индикатор обесцветится, лучи начнут проходить через раствор без поглощения я сила фототока в фотоэлементе резко увеличится. На графике сила тока - объем прилитой кислоты получают кривую с сильным перегибом. Этот перегиб соответствует эквивалентной точке. [16]
Метод основан на гашении люминесценции реагента в присутствии сульфид-ионов. Конечная точка титрования раствором реагента определяется графически из кривой зависимости интенсивности люминесценции от объема прибавленного раствора реагента. [17]
Этот метод основан на измерении оптической плотности раствора, которая является линейной функцией концентрации. При титровании вычерчивают кривую /) / ( и) ( где D - оптическая плотность раствора; v - объем прибавленного раствора - титранта), излом на которой соответствует точке эквивалентности. [18]
 |
Нахождение точки эквивалентности способом построения. а - касательных. б - зеркального изображения к касательной. [19] |
При титровании в водных растворах достаточно сильных кислот и оснований точке эквивалентности соответствует определенная величина рН, обычно непосредственно указываемая приборами рН - метрами. При титровании в неводных растворах или с помощью приборов, указывающих на изменение потенциала в процессе титрования, точка эквивалентности устанавливается по потенциометрической кривой, выражающей зависимость изменения потенциала индикаторного электрода от объема прибавленного раствора титранта. [20]
Хлористый натрий по Фольгарду определяют способом обратного титрования. Объем прибавленного раствора AgNO3 должен быть в полтора-два раза больше, чем нужно для полного осаждения всех ионов СР. Образуется осадок AgCl, а некоторая часть AgNO3 остается в свободном состоянии. [21]
В коническую колбу вместимостью 50 мл помещают 10 мл испытуемого 1 % - ного раствора. К этому раствору добавляют по каплям раствор одной из перечисленных солей до образования помутнения или выпадения осадка. При помутнении или выпадении осадка отмечают объем прибавленного раствора и содержимое колбы нагревают до кипения. Если раствор при этом осветляется, то добавляют еще не более 10 мл раствора соли или, когда осадок больше не образуется и раствор не пенится, добавление раствора прекращают. [22]
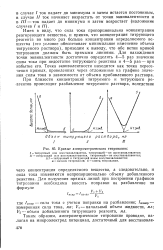 |
Кривые амперометрического титрования. [23] |
Имея в виду, что сила тока пропорциональна концентрации реагирующего вещества, и приняв, что концентрация титрующего реагента во много раз больше концентрации определяемого вещества ( это условие обеспечивает минимальное изменение объема титруемого раствора), приходим к выводу, что обе ветви кривой титрования должны быть прямыми линиями. Для нахождения точки эквивалентности достаточно определить 4 - 5 раз значение силы тока при недостатке титрующего реактива и 4 - 5 раз - при избытке его. Точка эквивалентности находится как точка пересечения прямых, проведенных через отложенные на графике значения силы тока в зависимости от объема прибавленного раствора. [24]
Имея в виду, что сила тока пропорциональна концентрации реагирующего вещества, и приняв, что концентрация титрующего реагента во много раз больше концентрации определяемого вещества ( это условие обеспечивает минимальное изменение объема титруемого раствора), приходим к выводу, что обе ветви кривой титрования должны быть прямыми линиями. Для нахождения точки эквивалентности достаточно определить 4 - 5 раз значение силы тока при недостатке титрующего реактива и 4 - 5 раз-при избытке его. Точка эквивалентности находится как точка пересечения прямых, проведенных через отложенные на графике значения силы тока в зависимости от объема прибавленного раствора. [25]
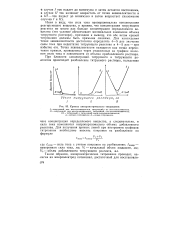 |
Кривые амперометрического титрования. [26] |
Имея в виду, что сила тока пропорциональна концентрации реагирующего вещества, и приняв, что концентрация титрующего реагента во много раз больше концентрации определяемого вещества ( это условие обеспечивает минимальное изменение объема титруемого раствора), приходим к выводу, что обе ветви кривой титрования должны быть прямыми линиями. Для нахождения точки эквивалентности достаточно определить 4 - 5 раз значение силы тока при недостатке титрующего реактива и 4 - 5 раз - при избытке его. Точка эквивалентности находится как точка пересечения прямых, проведенных через отложенные на графике значения силы тока в зависимости от объема прибавленного раствора. [27]
Имея в виду, что сила тока пропорциональна концентрации реагирующего вещества, и приняв, что концентрация титрующего реагента во много раз больше концентрации определяемого вещества ( это условие обеспечивает минимальное изменение объема титруемого раствора), приходим к выводу, что обе ветви кривой титрования должны быть прямыми линиями. Для нахождения точки эквивалентности достаточно определить 4 - 5 раз значение силы тока при недостатке титрующего реактива и 4 - 5 раз-при избытке его. Точка эквивалентности находится как точка пересечения прямых, проведенных через отложенные на графике значения силы тока в зависимости от объема прибавленного раствора. [28]
Метод основан на кроваво-красном окрашивании роданистого железа. Прокаленные окислы А12О3 - J - Fe2O3 ( см. выше) сплавляют с несколькими кристалликами кислого сернокислого калия, растворяют, к раствору прибавляют 2 - 3 мл 10 / 0-ного раствора роданистого калия и разбавляют до определенного объема. Приливают затем из бюретки к раствору роданистого калия, примерно одинаковой концентрации и объема, столько раствора железоаммониевых квасцов, чтобы в одинаковых объемах исследуемых растворов установилась одинаковая окраска. Искомое содержание железа дается объемом прибавленного раствора железоаммониевых квасцов. [29]
Обычно для определения МАВ находят теплоту смачивания или определяют величину нерастворяющего объема. При этом целесообразно применять соли хлора, так как ионы его легко определяются химическим способом. По изменению концентрации соли, объему прибавленного раствора, количеству воды в навеске воздушно-сухой почвы вычисляют предельно возможное содержание воды, связанной навеской. [30]
Страницы: 1 2 3