Калориметрическое определение
Cтраница 3
Однако и для калориметрического определения теплотворной способности топлива необходимо отобрать представительную среднюю пробу. Поэтому определение теплотворной способности топлива представляет известные трудности и для предприятий, располагающих лабораторными калориметрическими установками. [31]
Из различных методов калориметрического определения тепловых эффектов химических реакций наибольшее значение имеет метод определения теплот сгорания, до недавнего времени использовавшейся почти исключительно при исследовании органических соединений. Теперь он приобрел большое значение в термодинамике и неорганических соединений как один из основных источников данных по теплотам образования некоторых окислов ( при сжигании в атмосфере кислорода) и фторидов ( при сжигании в атмосфере фтора), а также для косвенного определения теплот образования других веществ. [32]
Рассмотрим в качестве примера калориметрическое определение теплот кислотно-основного взаимодействия в растворах этилендиаминтетрауксусной кислоты. [33]
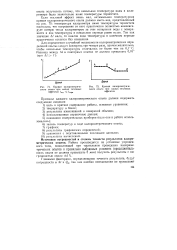 |
Кривая калориметрического опыта при малых тепловых эффектах. [34] |
Для определения случайной погрешности калориметрических определений опыты следует повторять три-четыре раза, причем желательно, чтобы начальные температуры отличались не более чем на 0 1 С. [35]
НИИнефтехим) разработана методика калориметрического определения 2 4-дихлорфенола в воздухе рабочих помещений производства 2 4 - Д на Уфимском химзаводе; методика калориметрического и нефелометрического определения а - метилстиро-ла в воздухе рабочих помещений производства - метилстирола и его использования на Уфимском заводе синтезспирта и Стерлитамакском заводе СК. [36]
Для определения случайной погрешности калориметрических определений опыты следует повторять три-четыре раза, причем желательно, чтобы начальные температуры отличались не более чем на О, Г С. [37]
Важно установить связь между абстрактным и элементарным калориметрическим определением теплоты. Калориметрическая единица теплоты, калория, определяется как количество теплоты, необходимое для повышения температуры 1 г воды от 14 до 15 С при атмосферном давлении. Таким образом, для того, чтобы повысить температуру т граммов воды от 14 до 15 С при атмосферном давлении, требуется т калорий теплоты. Пусть Дыс означает изменение энергии 1 г воды, а / с - работу, проделанную в результате ее расширения, когда температура повышается от 14 до 15 С при атмосферном давлении. [38]
Наиболее распространенным путем исследований является калориметрическое определение теплот образования. Однако в данном случае имеют место огромные трудности. [39]
В книге рассматриваются общие вопросы калориметрических определений, анализируются различные модели калориметрических систем, в которых учитываются различия тепловых свойств отдельных частей системы, и выводятся уравнения связи температурного поля системы с физическими свойствами и геометрическими особенностями входящих в нее тел. Излагаются аналитические способы определения поправок на теплообмен. Оцениваются погрешности измерений тепловых величин, обусловленные термической инерцией термоприемника и условиями теплообмена. Обсуждается вопрос об образцовых веществах, служащих для градуировки калориметрических измерительных средств. [40]
Один из наиболее старых методов калориметрического определения количества теплоты заключается в измерении изменения во времени температуры воды определенной массы в калориметре, в который введен образец, выделяющий или поглощающий теплоту. Данный принцип реализуется в жидкостных калориметрах. Метод основан на том. [41]
Для второго образца были также произведены калориметрические определения, которые дали, конечно, пониженные результаты по сравнению с первым автополимером. Однако если в вести поправку в полученные числа на кислород, то получаются довольно сходящиеся результаты. [42]
Метод: термографический, тенаиметрический; калориметрическое определение A / / 3KC1 - VC13 из твердых солей. [43]
Метод: термографический, тензиметрический, калориметрическое определение ДЯ 3RbCl - VCl3 из твердых солей. [44]
Описание различной системы калориметррв, методика калориметрических определений, а также расчеты приводятся в специальных курсах. [45]
Страницы: 1 2 3 4