Палладий
Cтраница 3
Палладий по своему поведению при электрохимическом выделении водорода во многом похож на платину. Данные опыта ( токи обмена и наклон тафелевских прямых) указывают на заторможенность рекомбинации как на вероятную причину водородного перенапряжения. [31]
Палладий в рекомендованном растворе находится в виде прочного комплексного соединения, поэтому контактно на медной фольге не выделяется. В процессе меднения образцы, закрепленные на проволочках, периодически покачивают. [32]
Палладий и платина в компактном состоянии являются серебристо-белыми металлами с гранецентрированной кубической структурой кристаллической решетки. Они относятся к тяжелым тугоплавким металлам. [33]
Палладий был открыт в 1803 г. Виллостоном и назван в честь маленькой планеты ( астероида) Pallas, открытой в 1802 г. другом Волластона Олберсом. [34]
Палладий растворим в конц. Остальные платиновые металлы, за исключением рутения, родия и иридия, могут быть растворены в царской водке. Окисление Ru, Rh и Ir удается провести при повышенных температурах, например, при их нагревании с кислородсодержащей соляной кислотой. Важное значение имеет способность некоторых платиновых металлов; ( платины и, особенно, палладия, см. опыт 2) растворять значительные количества водорода. [35]
Палладий ( PdC12) не образует с хромотроповой кислотой заметно окрашенных соединений, но мешает открытию титана своей собственной окраской. [36]
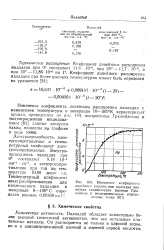 |
Изменение коэфициента линейного расширения палладия при низких температурах ( кривая Грю-нейзена и экспериментально определенные точки. [37] |
Палладий обладает значительно более высокой химической активностью, чем все остальные платиновые металлы. [38]
Палладий обладает замечательной способностью окклюдировать различные газы, причем более других газов способен поглощаться палладием водород. Ирм поглощении кислорода и окиси углерода палладий превращается в закись PdO. Гелий не поглощается палладием. Светильный газ, невидимому, не диффундирует через палладий или если диффундирует, то в незначительных количествах. [39]
Палладий - единственный металл платиновой группы, у которого поглощение водорода сопровождается образованием твердых растворов. [40]
Палладий способен поглотать, хотя 1 в меньшем объеме, также и изотоп водорода дейтерий. [41]
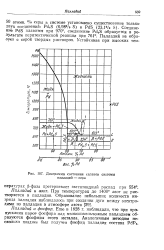 |
Диаграмма состояния сплавов системы палладий - сера. [42] |
Палладий не образует с серой твердых растворов. [43]
Палладий применяется в электротехнической, химической и ювелирной промышленностях. Чистый палладий применяется в электрических контактах в телефонном оборудовании для замены сплавов золота с платиной и серебром, так как, являясь более дешевым, о в то же время может применяться для боле -; высоких температур. [44]
Палладий - серебристо-белый металл, самый легкий из платиновых металлов, наиболее мягкий и ковкий. При этом палладий сохраняет металлический вид, но значительно увеличивается в объеме, становится ломким и легка образует трещины. Поглощенный палладием водород находится, по-видимому, в состоянии, приближающемся к атомарному, и поэтому очень активен. Насыщенная водородом пластинка палладия переводит хлор, бром и йод в галогеноводороды, восстанавливает соли железа ( III) в соли железа ( II), соли ртути ( II) в соли ртути ( I), диоксид серы в сероводород. [45]
Страницы: 1 2 3 4