Разложение - азотная кислота
Cтраница 3
Реакция образования нитрата аммония протекает с выделением значительного количества тепла, вследствие чего возникает опасность разложения азотной кислоты и азотнокислого аммония с образованием окислов азота. Чтобы предотвратить потери НМОз и NH4NO3, необходимо отводить или использовать выделяющееся тепло. Поэтому процесс получения аммиачной селитры ведут с использованием тепла реакции для испарения воды. [31]
 |
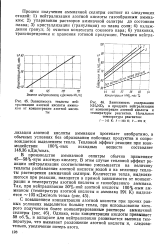
Схема концентрирования разбавленной азотной кислоты в присутствии серной кислоты. [32] |
Пары азотной кислоты с незначительным содержанием паров воды и окислов азота, образовавшихся в результате разложения азотной кислоты, направляются из колонны в холодильник-конденсатор 3, где азотная кислота конденсируется, а нитрозные газы ( окислы азота) идут на дальнейшее улавливание. [33]
Предположив, что концентрация ОН - - ионов стационарна, вывести уравнение для расчета скорости разложения азотной кислоты. [34]
Предположив, что концентрация ОН - - ионов стационарна, вывести уравнение для расчета скорости разложения азотной кислоты. [35]
 |
Строение клеточной мембраны. [36] |
В лабораторных условиях это превращение может быть осуществлено под действием оксидов азота, образующихся при разложении азотной кислоты при нагревании. [37]
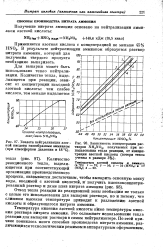
Однако, если концентрация кислоты превышает 58 об. %, в аппарате для нейтрализации развивается высокая температура, что вызывает разложение азотной кислоты и, следовательно, увеличение потерь азота. [39]
Однако если концентрация кислоты превышает 58 % HNO3, в аппарате для нейтрализации развивается высокая температура, что может приводить к разложению азотной кислоты и, следовательно, к увеличению потерь азота. [40]
Опасной представляется также передозировка концентрированной серной кислоты в азотную кислоту, так как за счет теплоты разбавления серной кислоты возможны локальные перегревы, вызывающие разложение азотной кислоты и аммиачной селитры, что также может приводить к образованию окислов азота и чувствительного к детонации нитрита в аппарате нейтрализации. Поэтому серную кислоту не рекомендуется дозировать в поток азотной кислоты перед нейтрализатором. Серную и азотную кислоты следует смешивать в отдельном аппарате; в нейтрализатор должна подаваться смесь кислот, предварительно подогретая до установленной регламентированной температуры и освобожденная от окислов азота. [41]
Таким образом, вначале идет процесс распада парафиновых углеводородов на свободные радикалы: R-R - 2R, а затеи последующее соединение их с продуктами разложения азотной кислоты: NO, NOj, Н2О в нитрозо -, нитро - и окснпарафииы. [42]
Поэтому понятно, что если взять два атома серной кислоты, то при возможно более осторожном нагревании, перегонка должна была бы проводиться без всякого разложения азотной кислоты. Однако на практике это невозможно, и никогда не удается при приготовлении концентрированной кислоты избежать образования красных паров. В начале этого процесса масса, содержащаяся в реторте, очевидно, представляет собой смесь жидкой кислоты и гранулированной соли. Однако это частичное разложение не представляет серьезного неудобства, ибо в хорошо охлаждаемом конденсаторе кислота образуется легко, и полученный продукт имеет лишь слабо желтун окраску. Именно по причине последнего обстоятельства на фабриках неохотно пойдут на использование двух атомов серной кислоты, ибо большие издержки совершенно не компенсируются. [43]
Отвод тепла реакции из реакционной зоны необходим не только с целью его использования для выпарки раствора, но и потому, что слишком высокая температура приводит к разложению азотной кислоты и образующегося нитрата аммония. [45]
Страницы: 1 2 3 4 5