Раствор - карбонат - калий
Cтраница 1
Растворы карбоната калия в воде имеют сильнощелочную реакцию. Из водных растворов кристаллизуется К2СОз - 1 5Н2О в виде блестящих стекловидных кристаллов, полностью теряющих воду при температуре 130 - 160 С. Карбонат гигроскопичен, при хранении на воздухе слеживается. [1]
Растворы карбоната калия применяются в текстильной промышленности при промывке шерсти для удаления из нее жиров. [2]
Раствор карбоната калия ( поташа) - при попадании на кожу или слизистую оболочку глаз вызывает раздражение. Попадание поташа в организм может вызвать тяжелое отравление. [3]
Растворы карбоната калия также являются коррозионнно-активны-ми по отношению к углеродистым сталям. [4]
Раствор карбоната калия с добавками ДЭА обладает хорошими смачивающими свойствами, и поэтому в нем задерживаются находящиеся в газе твердые частицы или распыленные жидкости. [5]
Как титруется раствор карбоната калия с фенолфталеином. [6]
Абсорбция сероводорода растворами карбоната калия или натрия представляет собой гетерогенный диффузионный процесс, сопровождающийся быстрой обратимой химической реакцией, протекающей в жидкой фазе. [7]
Препарат обрабатывают раствором карбоната калия, затем водой. После сушки над карбонатом калия и хлористым кальцием подвергают фракционной перегонке в токе сухого углекислого газа. [8]
К 50 мл раствора карбоната калия с концентрацией 3 моль / л и плотностью 1 30 г / мл медленно добавлено 35 7 мл 17 % - ного раствора хлорида цинка с плотностью 1 12 г / мл. [9]
К 50 мл раствора карбоната калия с концентрацией 3 моль / л и плотностью 1 30 г / мл медленно добавлено 35 7 мл 17 % - ного раствора хлорида цинка с плотностью 1 12 г / мл. [10]
Возможно применение в растворах карбоната калия в качестве активатора этаноламина вместо ДЭА. Недостатками этаноламина при этом являются более высокое давление насыщенных паров и связанная с ним необходимость промывки газа после очистки водой, однако этаноламин более доступен и дешев. [11]
 |
Схема установки для получения гидроксида натрия. [12] |
Для проведения реакции готовят раствор карбоната калия, растворив 50 г его в 50 г воды в химическом стакане. Через приготовленный раствор пропускают ток углекислого газа, полученного в аппарате Киппа. [13]
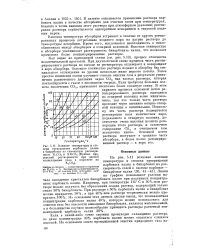
Легкость регенерации сероводорода из растворов карбоната калия зависит от общих условий процесса. Так, было показано [94, 95], что при температуре 110 С десорбция сероводорода протекает легче, чем двуокиси углерода. Отношение сероводород: двуокись углерода в поступающем на очистку газе оказывает на скорость адсорбции компонентов существенное влияние, которое до сего времени полностью не изучено. [14]
Страницы: 1 2 3 4