Твердый жидкий раствор
Cтраница 2
Диффузионные прослойки развиваются при сварке в момент сосуществования жидкой сварочной ванны с основным металлом вследствие разности растворимости углерода в твердом и жидком растворе железа. [16]
Совместимость Мк н Мп при пайке многообразна н проявляется при формировании паяного соединения в особенностях смачивания, растекания и затекания припоя в зазор, в процессах образования твердых и жидких растворов, развития общей и локальной химической эрозии паяемого металла, роста прослоек химических соединений, охрупчнвания паяемого металла, газовой, диффузионной и усадочной пористости. [17]
В зависимости от условий химической обработки и индивидуальных свойств исходные, промежуточные и образующиеся вещества могут быть представлены механической смесью индивидуальных компонентов или образованиями с различной формой связи компонентов в виде твердых и жидких растворов, а также фаз переменного состава. [18]
Активность чистой жидкости и чистого твердого тела при средних давлениях и температурах принимается за единицу. Активности компонентов в твердых и жидких растворах могут приниматься равными их молярной доле в растворе. [19]
Как уже указывалось выше, смешанные гидраты, образуемые бинарными и многокомпонентными смесями, в настоящее время рассматриваются как твердые растворы, состав которых изменяется при разложении гидрата. На основании аналогии между твердыми и жидкими растворами ( с точки зрения находящихся с ними в равновесии газовой или паровой фаз) Виль-кокс, Карсон и Катц [7] предложили метод вычисления условий образования гидратов из газовых смесей. [20]
ТЬ и Но близко расположены в ряду лантанидов ( 65ТЬ и 67Но) в металлическом состоянии имеют три коллективизированных валентных электрона ( 5d [ 6s2), изоструктурны ( имеют ГПУ решетку. Поэтому ТЬ и Но образуют почти идеальные твердые и жидкие растворы. [21]
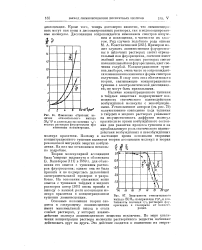
На рис. 136 а показано, как, пользуясь только что описанным методом, можно построить по кривым значений Z жидких и твердых растворов диаграммы состояния жидкий раствор - твердый раствор при постоянном давлении и переменной температуре. Буквами S и L обозначены соответственно кривые значений Z твердых и жидких растворов. [22]
На рис. 13б а показано, как, пользуясь только что описанным методом, можно построить по кривым значений Z жидких и твердых растворов диаграммы состояния жидкий раствор - твердый раствор при постоянном давлении и переменной температуре. Буквами S и L обозначены соответственно кривые значений Z твердых и жидких растворов. [23]
В интервале от Хд 0 52 - М, они образуют идеальный твердый раствор. В интервале Хд - 0 46 - Ю 52 смесь твердого и жидкого раствора стабильна. Постройте аккуратно кривую активности В во всем концентрационном интервале, используя чистый твердый металл в качестве стандартного состояния. [24]
Наличие концентрационного тушения в твердых веществах подразумевает возможность статического взаимодействия возбужденной молекулы с невозбужденными. Установленное автором ( см. рис. 79) количественное совпадение хода тушения в твердых и жидких растворах указывает на несущественность диффузии молекул красителя во время возбужденного состояния для развития процесса тушения и на преобладающую роль статического взаимодействия возбужденных и невозбужденных молекул красителя. Поэтому в настоящее время основными теориями концентрационного тушения являются теория ассоциации молекул и теория резонансной миграции энергии возбуждения. [26]
Сушка, обжиг, спекание, катализ, саморазвивающийся высокотемпературный синтез, охлаждение расплава, криохимическая обработка сопровождаются химическими взаимодействиями или полиморфными превращениями твердых простых веществ и соединений, входящих в обрабатываемую систему. Термодинамическими методами [199] устанавливают вероятность и параметры твердофазных и гетерогенных взаимодействий и превращений, выявляют вклад в константу равновесия твердых индивидуальных компонентов, твердых и жидких растворов, газовой фазы, а также оценивают свойства образующихся продуктов. [27]
Такое ограничение является общепринятым для первого этапа термодинамического исследования. Расчеты для реакций в стандартных условиях дают отправные точки, исходя из которых будет возможно впоследствии переходить к другим температурам и к более сложным системам, содержащим твердые и жидкие растворы, газовые смеси и кристаллические вещества сложного состава, как, например, алюмосиликаты и браун-миллерит, присутствие которых в прокаленных массах констатировалось некоторыми исследователями. [28]
Результаты термодинамического расчета реакции (6.7) показывают, что при пониженном давлении она заканчивается при температуре ниже 1800 С. Такой расчет фактически является очень большим упрощением, поскольку в системе ( оксиды урана) - ( углерод) протекает множество промежуточных химических реакций, приводящих ( см. рисунки 6.2 - 6.4) к образованию низших оксидов урана, карбидов, оксикарбидов, твердых и жидких растворов. [29]
Наиболее перспективным использованием таких расчетов является уточнение кривой солидус по кривой ликвидус п ограниченному набору термодинамических данных. Примером может служить расчет растворимости цинка в твердом кадмии по кривой ликвидус и свойствам жидких сплавов [ 7, с. Для случая непрерывных твердых и жидких растворов общие возможности корректных расчетов показаны в [34], хотя при анализе конкретных систем автор этой работы пренебрегал избыточными энтропиями смешения твердых растворов. [30]
Страницы: 1 2 3