Растворимость - сульфат - аммоний
Cтраница 1
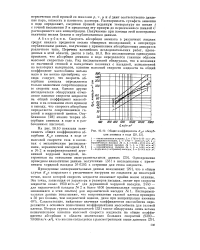 |
Общие коэффициенты KGa абеорб-ции аммиака в воде. [1] |
Растворимость сульфата аммония в воде определяют, соединяя прямой заданную температуру по шкале t с точкой насыщения S и продолжая эту прямую до пересечения со шкалой С растворимости или концентрации. Получаемые при помощи этой номограммы величины весьма близки к опубликованным данным. [2]
Растворимость сульфата аммония в слабых растворах серной кислоты ( 6 - 12 %) примерно такая же, как и в воде. [3]
Растворимость сульфата аммония в воде показана на рис. 5.23; он не образует кристаллогидратов, и его растворимость мало изменяется при повышении температуры. Сульфат аммония применяют почти исключительно в качестве удобрения; он обладает весьма небольшой гигроскопичностью, мало слеживается, внесение его в почву не вызывает затруднений. Недостатками являются низкое содержание азота и большая физиологическая кислотность. При его применении в почве, если она не содержит достаточного количества оснований, постепенно накапливается серная кислота, для нейтрализации которой необходимо периодически производить известкование. [4]
 |
Удельный вес водных растворов сульфата аммония. [5] |
Растворимость сульфата аммония в слабых растворах серной кислоты ( 5 - 10 %) примерно такая же, как и в воде. [6]
Из таблицы видно, что растворимость сульфата аммония Б воде мало изменяется с температурой. В водных растворах аммиака растворимость сульфата аммония значительно снижается. [7]
Метод выделения сульфата аммония из раствора, насыщенного аммиаком, основан на том, что растворимость сульфата аммония в водных растворах аммиака значительно уменьшается по сравнению с растворимостью в воде. При этом растворимость смол не изменяется. Поэтому при насыщении охлажденного раствора сульфата аммония аммиаком происходит кристаллизация сульфата аммония, который выделяется из раствора, захватывая лишь небольшое количество примесей. Недостатком этого метода является большая энергоемкость и малая степень извлечения. [8]
Метод выделения сульфата аммония из раствора, насыщенного аммиаком, основан на том, что растворимость сульфата аммония в водных растворах аммиака значительно уменьшается по сравнению с растворимостью в воде. При этом растворимость смол не изменяется. [9]
 |
Политерма системы ( NH4 aSO4 - Н8О. [10] |
Сульфат аммония ( NH4) aSO4 - - бесцветное кристаллическое вещество ( плотность 1769 кг / м3), содержит 21 21 % азота, при нагревании выше 350 С разлагается на аммиак и серную кислоту; частичное разложение с образованием кислых солей начинается выше 200 С. Растворимость сульфата аммония в воде показана на рис. 96; он не образует кристаллогидратов, и его растворимость мало изменяется при повышении температуры. Сульфат аммония применяют почти исключительно в качестве удобрения; он обладает весьма небольшой гигроскопичностью, мало слеживается, внесение его в почву не вызывает затруднений. Недостатком является большая физиологическая кислотность. При его применении в почве, если она не содержит достаточного количества оснований, постепенно накапливается серная кислота, для нейтрализации которой необходимо периодически производить известкование. [11]
Из таблицы видно, что растворимость сульфата аммония Б воде мало изменяется с температурой. В водных растворах аммиака растворимость сульфата аммония значительно снижается. [12]
Сульфат аммония нерастворим в абсолютном алкоголе и ацетоне. В водных растворах аммиака растворимость сульфата аммония значительно снижается с увеличением содержания аммиака. [13]
Знание степени пересыщения раствора позволяет учитывать особенности первичного и вторичного зародышеобразования, а также заранее рассчитать время роста кристаллов до заданного размера. При использовании различного рода добавок необходимо учитывать степень их влияния на растворимость сульфата аммония. Последнее нужно прежде всего для корректирования данных о степени пересыщения раствора. [14]
Сульфат аммония представляет собой хорошо растворимую соль. В 100 г Н2О при О С растворяется 70 1 г ( NH4) 2SO4, а при 100 С - 102 г. Как видим, растворимость сульфата аммония обладает сравнительно небольшим температурным коэффициентом. Поэтому термическим способом могут быть достигнуты небольшие пересыщения. Сульфат аммония кристаллизуется в виде бесцветных кристаллов, относящихся к ромбической сингонии. Будучи одним из распространенных удобрений, сульфат аммония привлекал и привлекает внимание исследователей. Практически изучаются все стороны его поведения при образовании осадков. [15]
Страницы: 1 2