Ветвь - кристаллизация
Cтраница 3
Эвтектика; твердые фазы: КС1, KsSO Ветви кристаллизации почти прямолинейны, со слабой выпуклостью к оси составов. [31]
На кривой ли - (, С квидуса имеется ветвь кристаллизации инконгруэнтно плавящегося при 240 соединения неустановленного состава. Для составов, содержащих менее 7 % 1паС13, наблюдается расслаивание. [32]
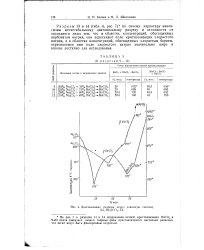 |
Диагональные разрезы через взаимную систему Na, Ba ] CO3, C1. [33] |
На рис. 7 в разрезах 13 и 14 направление ветвей кристаллизации ВаСО3 и NaCl почти совпадает; однако твердые фазы кристаллизуются настолько различно, что легко могут быть фиксированы визуально. [34]
Установлены составы жидких фаз в узловых точках и па ветвях кристаллизации, ограничены поля кристаллизации солей. [35]
При 0 в исследуемой системе наблюдается минимум растворимости фторида на ветвях кристаллизации КНР. [36]
 |
Диаграммы плавкости системы С1207 - S03 - Н20 ( а и разреза Н2804 - НС104 ( б. [37] |
Разрез НСЮ4 - H2S04 в результате отсутствия дистектической точки и даже ветви кристаллизации для соединения НСЮ4 в системе С1207 - Н2О не является бинарным. [38]
 |
Изотерма растворимости солей. [39] |
Сопоставление ветвей растворимости и характер выделения чистых компонентов показывает, что хлорид лития имеет относительно меньшую ветвь кристаллизации, чем хлорид натрия. [40]
Исследование политермических сечений, пересекающих вершины исходных солей, дает возможность по двум-трем термограммам составов, принадлежащих ветви кристаллизации добавляемого компонента, определить однозначно, кроме ветви кристаллизации этого компонента, также и температуру, и состав точек пересечения кривых кристаллизации. По совокупности данных двух подобных сечений определяется кривая моновариантных равновесий в тройной или тройной взаимной системе, а также температура и состав тройной эвтектической точки. [41]
Исследование политермических сечений, пересекающих вершины исходных солей, дает возможность по двум-трем термограммам составов, принадлежащих ветви кристаллизации добавляемого компонента, определить однозначно, кроме ветви кристаллизации этого компонента, также и температуру, и состав точек пересечения кривых кристаллизации. По совокупности данных двух подобных сечений определяется кривая моновариаптпых равновесий в тройной или тройной взаимной системе, а также температура и состав тройной эвтектической точки. [42]
Из табл. 1 видно, HTOS изотерма растворимости системы NaNOs - Na2CO3 - Н2О состоит из двух ветвей кристаллизации: декагидрата Na2CO3 - 10H2O и нитрата натрия. [43]
 |
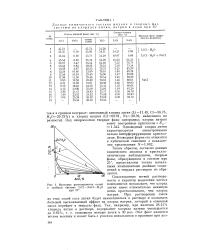
Изотермы растворимости системы H2SC4 - Na2SO4 - H2O при 0 и 25. [44] |
Из рис. 4 видно, что пересечение этой пограничной линии с изотермой 0 может осуществиться в точке, которая лежит не на реально полученной ветви кристаллизации десятиводного сульфата натрия, а на ее продолжении. Отсюда можно заключить, что ветвь кристаллизации Na2SO4 10Н2О прерывается ветвью кристаллизации кислой соли Na3H ( SO4) 2 раньше, чем она могла дойти до поля кристаллизации сульфата натрия. По этой причине при 0 стабильная ветвь кристаллизации безводного сульфата натрия отсутствует вовсе. [45]
Страницы: 1 2 3 4