Скорость - диффузия
Cтраница 3
Скорость диффузии определяется количеством вещества т, диффундирующего через единицу площади поверхности раздела за единицу времени. Количество диффундирующего ( в единицу времени) вещества т зависит от градиента концентрации dtldx элемента в направлении, нормальном к поверхности раздела и пропорционально коэффициенту диффузии D: т - D ( dCldx), где dC - концентрация; dx - расстояние в выбранном направлении. [31]
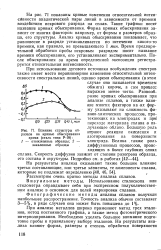 |
Влияние структуры об - илрают реакции окисления и разцов на кривые обыскривания v v. [32] |
Скорость диффузии зав йсит от степени разогрева образца, его состава и структуры. [33]
Скорости диффузии их низки, и обычно они не могут мигрировать на большие расстояния, что, однако, является необходимым условием приведения кристалла в состояние равновесия с внешней средой при обычных температурах. Для достижения равновесия приходится повышать температуру, но в таком случае результаты измерений концентрации электронов и дырок, выполненных при низких температурах, следует интерпретировать достаточно осторожно, так как концентрации дефектов, характерные для высокой температуры, отличаются от измеренных экспериментально. В зависимости от скорости охлаждениями скорости диффузии значения концентраций могут быть промежуточными между равновесными и измеренными при данной температуре. [34]
Скорость диффузии по междоузлиям в значительной степени определяется размером атома и параметрами решетки как на стадии перехода атома из узла в междоузлие, так и при его движении между двумя междоузлиями. Скорость диффузии по описанным выше механизмам целиком определяется концентрацией дефектов. В условиях термического равновесия имеется определенная концентрация этих дефектов в кристалле ( см. разд. [35]
Скорости диффузии в модифицированных и обычных ионитах с одинаковым количеством дившшлбензола практически совпадали. [36]
Скорость диффузии ( проникновения) R описывается уравнением: nRaT - b, где Т - абсолютная температура; а и b - эмпирические константы. [37]
Скорость диффузии в двух жидкостях значительно меньше, и поэтому при экстракции необходимо более совершенное разделение веществ на тонкие слои, чем при ректификации. Однако тонкое разделение препятствует расслоению, которое должно осуществляться на каждой ступени. [38]
 |
Схема, поясняющая уравнение диффузии. [39] |
Скорость диффузии в приэлектродном слое, совершающейся в направлении оси х между двумя сечениями д, находящимися на расстоянии dx ( рис. 99), дается известным уравнением Фика ( гл. [40]
 |
Диффузионное пламя горения углеводородов в воздухе. [41] |
Скорость диффузии при этом характеризует скорость горения углеводородов в пламени. Такое пламя называют диффузионным, оно бывает ламинарным и турбулентным. [42]
Скорость диффузии и накопления водорода зависит от структуры стали: она велика в феррите и мартенсите, незначительна в аустените. В результате дополнительных внутренних напряжений в металле мартенситные включения увеличивают склонность стали к коррозионному растрескиванию под напряжением. Мартенсит закалки имеет неравновесную структуру, тетрагональную решетку, игольчатое строение, высокую твердость и характеризуется наличием внутренних напряжений. Они повышаются с увеличением содержания в сплаве С, Mn, Ni, с увеличением твердости, предела - текучести и величины напряжений. [43]
Скорость диффузии при этом увеличивается, а следовательно, значительно увеличивается и скорость процесса взаимодействия между компонентами с образованием новой кристаллической фазы. Не исключена возможность, что образованию новой кристаллической фазы под влиянием высокой температуры предшествует процесс удаления из решетки твердого тела отдельных атомов и молекул, что приводит к появлению молекулярно-пористых тел, образующих псевдоморфозы по исходным кристаллам. Появление молекулярно-пористых тел существенно влияет на захват твердыми телами сульфата кальция, введенного в цементную шихту, и приводит к значительному контактированию между компонентами. [44]
 |
Схема гель-хроматографии. [45] |
Страницы: 1 2 3 4 5