Весьма устойчивое соединение
Cтраница 2
Все известные способы получения ХТНФ основаны на удалении воды из растворов гипохлорита натрия с помощью полностью или частично обезвоженного тринатрийфосфата. При этом образуется весьма устойчивое соединение, сохраняющее активный хлор в течение продолжительного времени. [16]
В природе воски распространены довольно широко, но содержатся в небольших количествах, это затрудняет их получение и техническое использование. Они являются химически весьма устойчивыми соединениями. Гидролизуются они значительно труднее, чем глицериды. [17]
Полученный нами 4-метилкамфолид оказался весьма устойчивым соединением; он не давал продуктов расщепления ни с цианистым калием, ни с уксуснокислым раствором бромистого водорода. [18]
 |
Данные о полимеризации на фосфорнокислотных катализаторах. [19] |
По-видимому, эта активность обусловлена образованием комплексного весьма устойчивого соединения - силикофосфата. [20]
Ниже описываемый способ пригоден для получения также и других комплексов с ароматическими лигандами, например с бензолом, толуолом и ксилолом. Промежуточно образующийся гексакарбонилванадатный комплекс может быть выделен и представляет собой термически весьма устойчивое соединение. [21]
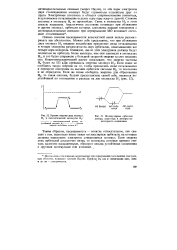 |
Уровни энергии двух молекул, 53. Молекулярные орбитали. [22] |
Таким образом, насыщаемость - понятие относительное, оно свя-зано с тем, насколько низко лежат молекулярные орбитали, на которые должны переходить электроны сливающихся молекул. Если энергия этих орбиталей достаточно низка, то молекулы, которые принято считать валентно насыщенными, образуют весьма устойчивые соединения с другими молекулами или атомами. [23]
Долгое время, когда уже производили простейшую переработку нефти, выделяя из нее в перегонных кубах отдельные фракции, углеводороды считали химически инертными веществами. При высокой температуре они, конечно, разлагались и сгорали, но ниже температур разложения и воспламенения углеводороды рассматривались как весьма устойчивые соединения, и казалось не реальным производство из них каких-либо полезных продуктов. [24]
Однако для человека главная угроза со стороны фтора как токсиканта природной среды заключается совсем в другом. Дело в том, что в результате применения хлор-или фтор-органических соединений в качестве хладагентов и газов-вытеснителей в холодильниках и аэрозольных баллонах они попадают в атмосферу; будучи весьма устойчивыми соединениями, эти легкие газы поднимаются все выше в тропосферу и даже в стратосферу. В связи с этим возникает опасение, что там под воздействием атомов хлора может начаться процесс каталитического расщепления Оз и в результате может быть полностью или хотя бы частично разрушен слой озона. Самое меньшее, что тогда могло бы ожидать нас в будущем - это, вероятно, рост заболеваемости раком кожи, так как сейчас слой озона надежно защищает нас от ультрафиолетового излучения Солнца. [25]
Анилин содержит два весьма различных по характеру реакционных центра - аминогруппу и ароматическое ядро. Поэтому избирательно защитить один из них не составляет проблемы. Продукт реакции - ге-нитроанилин - весьма устойчивое соединение и легко переживает условия достаточно жесткого щелочного гидролиза. В химии углеводов дело обстоит несравненно сложнее. Прежде всего, здесь функциональные группы весьма сходны, так что ввести защиту избирательно - а в этом весь смысл такой операции - весьма непросто. Таких групп в молекуле несколько ( чтобы не сказать, много), а защитить нужно все, кроме одной-двух. Понятно, что это обстоятельство, вообще говоря, не упрощает задачу. Наконец, сами углеводы и практически все их производные - соединения достаточно высоко реак-ционноспособные. [26]
Было испробовано множество методов. В фталоцианин меди вводились заместители, позволяющие осуществлять кубовое крашение, с тем чтобы можно было обрабатывать хлопок лейкосоедине-нием, так же как при применении кубовых красителей - каледонов. К сожалению, фталоцианин меди, являющийся вообще-то весьма устойчивым соединением, не обладает устойчивостью к восстановительному процессу, применяемому при кубовом крашении. Эти красители имеют не синий, а зеленый цвет, и, хотя один из них нашел сбыт на рынке, задача окраски хлопчатобумажных тканей в присущей фталоцианину меди цвет оставалась нерешенной. [27]
Было испробовано множество методов. В фталоцианин меди вводились заместители, позволяющие осуществлять кубовое крашение, с тем чтобы можно было обрабатывать хлопок лейкосоедине-ннем, так же как при применении кубовых красителей - каледонов. К сожалению, фталоцианин меди, являющийся вообще-то весьма устойчивым соединением, не обладает устойчивостью к восстановительному процессу, применяемому при кубовом крашении. Эти красители имеют не синий, а зеленый цвет, и, хотя один из них нашел сбыт на рынке, задача окраски хлопчатобумажных тканей в присущей фталоцианину меди цвет оставалась нерешенной. [28]
Хорнер и сотрудники показали, что трифенилдихлорфос-фор реагирует с амидами карбоновых кислот только в присутствии триэтиламина. При этом образуются окись трифенилфосфина и нитрилы карбоновых кислот, а трифенилфосфазокарбацилы не получаются вовсе. Можно было предполагать, что образующиеся вначале трифенилфосфазокарбацилы термически нестойки и в условиях реакции разлагаются на нитрилы и окись трифенилфосфина. Однако полученные другим путем ( см. 3.1.7.) трифенилфосфазокарбацилы оказались весьма устойчивыми соединениями. Следовательно, они не являются промежуточными продуктами реакции трифенилдихлорфосфора с амидами кислот. [29]
Двуокись плутония является очень стабильным соединением, теплота образования которого - 246 5 ккал / молъ. При высоких температурах может происходить отщепление кислорода с образованием фазы Ри203, что является следствием большей устойчивости более низкого состояния окисления плутония. На основании большой величины теплоты образования двуокиси плутония можно сделать вывод о том, что РиО2 не должна восстанавливаться водородом до металлического состояния. Ожидаются следующие реакции с РиО2: фторирование HF должно приводить к образованию либо PuF3, либо PuF4, а галогенирование - к образованию тригалогенидов плутония; при взаимодействии с сероводородом должны образовываться сульфиды плутония, при взаимодействии с избытком углерода - карбиды. Прокаленная двуокись плутония является весьма устойчивым соединением и может быть растворена лишь с большим трудом. Для растворения РиОг рекомендуется сплавлять ее с пиросульфатом калия или нагревать в концентрированной азотной кислоте с добавлением 0 005 молъ / л плавиковой кислоты. Окись, приготовленная при низкой температуре, легко растворяется в горячей концентрированной серной или азотной кислоте. [30]
Страницы: 1 2 3