Влияние - молекулярный кислород
Cтраница 1
Влияние молекулярного кислорода на интенсивность, ширину и форму линии спектра ЭПР было исследовано на продуктах РТМ поливинилацетата в диапазоне от 400 до 700 С и на продуктах термической обработки полиэтилена, полученных как стандартным 2-часовым предокислением и последующей обработкой в вакууме при 720 С в течение 0 6 часа, 1 часа, 2 час. [1]
Влияние молекулярного кислорода на заедание стали в присутствии растворов и эмульсий присадок в полиорганосилоксанах Проявляется различно в зависимости от природы этих соединений. В работе высказано предположение, что эффективность присадок против заедания определяется процессами, в которых участвуют свободные радикалы, причем важную роль в этих процессах играет базовое масло. Этим может быть объяснена низкая приемистость полиорганосилоксанов по отношению к присадкам рассмотренного типа, которые весьма эффективны в углеводородных смазочных средах. [2]
Характер влияния молекулярного кислорода на процессы, протекающие под действием обычных радикальных инициаторов, определяется относительной активностью данного мономера. [3]
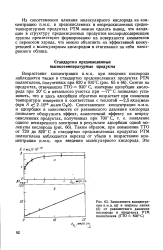 |
Зависимость концентрации п.м.ц. ( а и ширины линии ( б от равновесного давления кислорода в продуктах РТМ полиэтилена ( ТТО 820 С. [4] |
Из сопоставления влияния молекулярного кислорода на концентрацию п.м.ц. в предокисленных и непредокисленных средне-температурных продуктах РТМ можно сделать вывод, что входящие в структуру предокисленных продуктов кислородсодержащие группы препятствуют формированию на поверхности комплексов с переносом заряда, что можно объяснить их эффективной конкуренцией с молекулярным кислородом в стягивании на себя электронного облака. [5]
Для выяснения влияния молекулярного кислорода па поведение продуктов реакции была проведена другая серия опытов в том же сосуде. В этой серии опытов струя проходила, минуя трубку, наполненную J205; скорость струи в этой серии составляла примерно 200 - 250 см / сек. На рис. 4 представлены кривые накопления СН20, СО и С02, построенные по опытным данным второй серии опытов. [6]
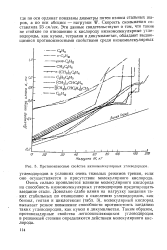 |
Противоизносные свойства низкомолекулярных углеводородов. [7] |
Очень сильно проявляется влияние молекулярного кислорода на способность низкомолекулярных углеводородов предотвращать заедание стали. Довольно слабо влияя на нагрузку заедания таких стабильных по отношению к окислению углеводородов, как бензол, гептан и циклогексан ( табл. 3), молекулярный кислород вызывает резкое повышение способности противостоять заеданию таких углеводородов, как кумол и дикумилметан. Таким образом, противозадирные свойства легкоокисляющихся углеводородов в решающей степени определяются действием молекулярного кислорода. [8]
В этой работе экспериментально изучено влияние молекулярного кислорода, перекисей ( органических и неорганических), солей серебра, меди и других сокатализаторов на каталитическую активность металло-органических соединений бора, кадмия, цинка и алюминия. Показано, что поведение кислородных соединений связано с природой центрального атома металлоорганического соединения. [9]
Автоокислением принято называть окислительные процессы, совершающиеся самопроизвольно под влиянием молекулярного кислорода. [10]
Альдегиды очень хорошие восстановители, так как легко окисляются, иногда даже под влиянием молекулярного кислорода. [11]
Рассмотренные в этой главе теоретические представления о природе окислительных процессов, совершающихся под влиянием молекулярного кислорода, позволяют сделать ряд обобщений, которые можно трактовать как современную точку зрения на механизм этих явлений, в частности на механизм медленного окисления углеводородов. [12]
Эти полимеры вырастают из зародышей, образующихся при очень медленной реакции, по-видимому, под влиянием молекулярного кислорода, причем сначала образуются полимерные перекиси. Активные зародыши, имеющие форму зерна, могут вызвать дальнейший рост не только диенов, но и моно-винильных соединений; при этом получаются совершенно нерастворимые, но еще набухающие продукты. [13]
Механизм действия параквата заключается в том, что катион под влиянием хлорофилла восстанавливается до сравнительно устойчивого свободного радикала и снова окисляется под влиянием молекулярного кислорода. При этом образуется перекись водорода, которая накапливается в растениях в фитотоксических концентрациях. В почве паракват подвержен быстрой необратимой адсорбции путем включения в глинистые минералы. Следовательно, это соединение не включается в пищевую цепь и таким образом не вызывает вторичных токсикологических эффектов и не загрязняет окружающую среду. [14]
Перекисные соединения, главным образом перекись водорода и надуксусная кислота ( а в последнее время-и гидроперекиси), получили применение как окислительные агенты в основном органическом и нефтехимическом синтезе сравнительно недавно. Ввиду относительной дороговизны их используют только для таких реакций, которые под влиянием молекулярного кислорода или азотной кислоты не протекают. [15]
Страницы: 1 2