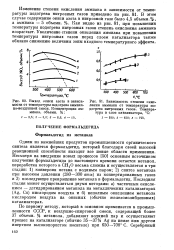
Температура - нитрозный газ
Cтраница 2
Необходимость охлаждения зоны поглощения следует хотя бы из того, что температура нитрозного газа, содержащего 10 % NO, только вследствие протекания реакции окисления NO в NO2 может повыситься до 200 С. [16]
Газы, выходящие из доокислителя при 40 С, охлаждаются в холодильнике рассолом до - 10 С, причем на участке между второй окислительной башней и рассольным холодильником температура нитрозных газов несколько снижается. [17]
Далее они поступают в окислитель, в верхней части которого установлен фильтр для улавливания платины ( стекловата), затем последовательно они проходят подогреватель воздуха, где охлаждаются до 210 - 230 С, подогреватель хвостовых газов, где охлаждаются до 150 - 160 С, и холодильник-конденсатор, в котором температура нитрозных газов снижается до 45 - 50 С. Охлажденные нитрозные газы поступают в нижнюю часть абсорбционной колонны, представляющей собой аппарат диаметром 2, высотой 46 м, снабженный 49 ситчатыми тарелками. На тарелках уложены змеевики, в которые подается - оборотная вода для отвода тепла. На верхнюю тарелку подается охлажденный конденсат, который, двигаясь навстречу потоку нитрозных газов, поглощает окислы азота с образованием азотной кислоты. Полученная азотная кислота самотеком направляется в продувочную колонну, где при помощи горячего воздуха производится отдувка растворенных окислов азота, которые подаются на 6 - ю тарелку абсорбционной колонны. Хвостовые газы, выйдя из абсорбционной колонны, направляются через подогреватель хвостовых газов на каталитическую очистку. [18]
 |
Примерная схема производства слабой азотной кислоты под давлением 0 73 МПа. [19] |
Далее они поступают в окислитель, в верхней части которого установлен фильтр для улавливания платины ( стекловата), затем последовательно они проходят подогреватель воздуха, где охлаждаются до 210 - 230 С, подогреватель хвостовых газов, где охлаждаются до 150 - 160 С, и холодильник-конденсатор, в котором температура нитрозных газов снижается до 45 - 50 С. Охлажденные нитрозные газы поступают в нижнюю часть абсорбционной колонны, представляющей собой аппарат диаметром 2, высотой 46 м, снабженный 50 ситчатыми тарелками. На тарелках уложены змеевики, в которые подается оборотная вода для отвода теплоты. На верхнюю тарелку подается охлажденный конденсат воды, который, двигаясь навстречу потоку нитрозных газов, поглощает оксиды азота с образованием азотной кислоты. [20]
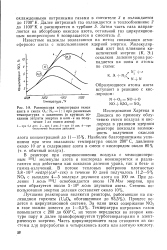 |
Равновесная концентрация окиси азота в смеси О2. N2 при различных температурах и давлениях ( в кружках показаны затраты энергии в кет ч на получение 1 кг окиси азота. [21] |
Процесс ведется в циркуляционной системе. Температура нитрозных газов повышается с 200 до 600 С, их тепло передается во втором контуре пару и далее трансформируется турбогенераторами в электрическую энергию. Часть циркулирующего газа отводится из системы для переработки в четырехокись азота или азотную кислоту. [22]
Подача воздуха, аммиака и добавочного кислорода осуществляется с помощью аммиачно-воздушного вентилятора 4 с таким расчетам, чтобы газовая смесь содержала 10 - 12 % МНз-Затем газовая смесь проходит поролитовый фильтр 7, в котором очищается путем фильтрации через трубки из пористой керамики, и сверху поступает в контактный аппарат 8, в средней части которого помешены платино-родиевые сетки ( см. рис. 47, гл. Температура нитрозных газов на выходе из контактного аппарата обычно поддерживается около 800 С. В котле-утилизаторе 9 температура газов снижается до 250 С. Затем газы охлаждаются водой в кожухотрубных холодильниках 10 и 11 примерно до 30 С. При этом происходит частичная конденсация водяных паров и окисление окиси азота. [23]
После реакции окисления аммиака нитрозные газы с температурой 1073 - 1093 К поступают в котел-утилизатор 15 для получения пара давлением 10 - 12 - 105 Па за счет утилизации тепла реакции. В результате получения пара температура нитрозных газов снижается с 1073 до 443 К - Для дальнейшего охлаждения нитрозные газы поступают в холодильник 17, по трубкам которого циркулирует охлаждающая вода. В отходящих нитрозных газах должно содержаться кислорода не менее 5 об. %, поэтому после газового холодильника непосредственно в газоход нитрозных газов через вентилятор 16 подается дополнительно воздух для обеспечения окисления NO в NO2 в абсорбционной зоне. [24]
 |
Нижний и верхний пределы взрываемости смесей 02, N2 и.| Нижний и верхний пределы взрываемости смесей NH3. [25] |
В производственных условиях за катализаторными сетками иногда наблюдается образование аммиачной селитры из непрореагировавшего аммиака. Нитрат аммония отлагается в последующей аппаратуре азотнокислотных систем при понижении температуры нитрозных газов. [26]
Из котла-утилизатора нитрозные газы, охлажденные до 443 К, направляются в окислитель 9, выполненный в виде полой башни. Нитрозные газы поступают в окислитель со степенью окисления до 40 %, в результате реакции окисления оксида ( II) NO до оксида ( IV) NO2 до 83 - 84 % температура нитрозных газов повышается до 573 - 583 К. В верхней части окислителя нитрозных газов установлен фильтр для улавливания платины, унесенной газами из контактного аппарата. После окислителя нитрозные газы температурой 583 К охлаждаются за счет нагрева воздуха в подогревателе воздуха 10 до 443 - 448 К. [27]
На некоторых производствах азотной кислоты комбинированным методом в систему автоматического регулирования включена вычислительная машина УМ-1 с 5000 кодов. На одном из действующих предприятий в такую машину заложена следующая программа: процент выполнения плана; себестоимость продукции; количество вводимого в цех аммиака; количество аммиака для очистки хвостовых нитрозных газов на ванадиевом катализаторе; расходные коэффициенты для пара, кислорода, химически очищенной, обессоленной, оборотной воды, электроэнергии; выработка кислоты; температура нитрозного газа после газового холодильника-промы-вателя; температура под первой тарелкой абсорбера. [28]
Окисление атмосферного азота научалось многими исследователями, но наиболее полно этот процесс описан в гл. Экспериментально показано влияние температуры плазмы, давления, отношения азота к кислороду на процесс образования окиси азота. Исследование процесса снижения температуры нитрозных газов позволило установить [73] закон закалки dT / dt f ( T), необходимый для сохранения 95 % образовавшегося количества окиси азота. [29]
Страницы: 1 2 3