Атомно-молекулярная теория
Cтраница 2
Основные положения атомно-молекулярной теории состоят в следующем. Все вещества состоят из химически неделимых частиц - атомов. В свою очередь, атомы могут соединяться между собой, образуя молекулы - частицы, состоящие из разного числа атомов. В противоположность атомам молекулы химически делимы. Химические реакции представляют собой разрушение одних молекул и образование других. Таким образом, молекулы являются наименьшими частицами индивидуального вещества, сохраняющими его химические свойства, его химическую индивидуальность. [16]
Логическим следствием атомно-молекулярной теории Ломоносова является одинаковость состава нечувствительных частиц ( молекул) с составом любой массы образованного из них вещества. [17]
Основные положения атомно-молекулярной теории сводятся к следующим. [18]
Основные положения атомно-молекулярной теории состоят в следующем. Все вещества состоят из химически неделимых частиц - атомов. В свою очередь, атомы могут соединяться между собой, образуя молекулы - частицы, состоящие из разного числа атомов. В противоположность атомам молекулы химически делимы. Химические реакции представляют собой разрушение одних молекул и образование других. Таким образом, молекулы являются наименьшими частицами индивидуального вещества, сохраняющими его химические свойства, его химическую индивидуальность. [19]
Таким образом, атомно-молекулярная теория через 100 с лишним лет возродила корпускулярную теорию Ломоносова. [20]
С точки зрения атомно-молекулярной теории закон сохранения массы веществ объясняется тем, что при химических реакциях общее количество атомов не изменяется, а происходит только их перегруппировка. А так как атомы имеют постоянную массу, то это и приводит к закону сохранения массы веществ. [21]
Толчком к созданию атомно-молекулярной теории явилось порожденное требованиями мануфактурного производства изучение жидкостей и газов. С одной стороны, развитие гидростатики и гидродинамики ( физика), а с другой - изучение процессов восстановления металлов и горение топлива ( химия) дали конкретные представления о строении веществ из атомов и молекул или корпускул. [22]
С точки зрения атомно-молекулярной теории, закон сохранения массы веществ объясняется тем, что при химической реакции происходит перегруппировка атомов из молекул исходных веществ в молекулы новых. Количество атомов при этом сохраняется, и поэтому общая масса всех атомов остается постоянной до и после реакции. [23]
С точки зрения атомно-молекулярной теории, атомный состав молекулы всегда постоянен, масса атома-также постоянная величина. [24]
С точки зрения атомно-молекулярной теории суть этого закона совершенно понятна. [25]
С точки зрения атомно-молекулярной теории химическим элементом называют совокупность атомов, имеющих определенную массу. [26]
С точки зрения атомно-молекулярной теории закон сохранения массы веществ заключается в следующем: при химической реакции происходит перегруппировка атомов из молекул исходных веществ в молекулы новых веществ. Количество атомов сохраняется, и поэтому общая масса всех атомов остается постоянной до и после реакции. [27]
С точки зрения атомно-молекулярной теории закон постоянства состава объясняется неизменяемостью массы атомов в процессе химической реакции и способностью атомов каждого элемента присоединять к себе определенное количество атомов другого элемента. [28]
Как известно из атомно-молекулярной теории строения вещества, молекула представляет собой объединение положительных и отрицательных заряженных частиц, которое само по себе электрически нейтрально. [29]
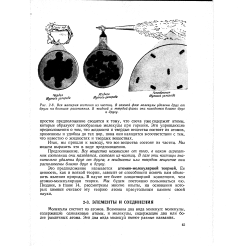 |
Вся материя состоит из частиц. В газовой фазе молекулы удалены друг от друга на большие расстояния. В жидкой и твердой фазах они находятся близко друг. [30] |
Страницы: 1 2 3 4