Торможение - катодный процесс
Cтраница 3
Непосредственное определение 9 и Дг для твердых металлов в настоящее время затруднительно, поэтому зависимости (2.17), (2.20), (2.23), (2.24) могут быть использованы лишь для качественных суждений о механизме торможения катодного процесса ингибиторами. [31]
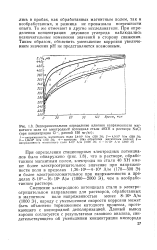 |
Экспериментальное определение влияния напряженности магнитного поля на электродный потенциал стали 40ХН в растворе МаС1 ( при концентрации С1 -, равной 150 мг / кг. [32] |
Смещение электродного потенциала стали в электроотрицательном направлении для растворов, обработанных в магнитном поле напряженностью менее 8 - Ю4 А / м ( 1000 Э), наряду с уменьшением скорости коррозии может быть объяснено торможением катодного процесса, протекающего с кислородной деполяризацией. [33]
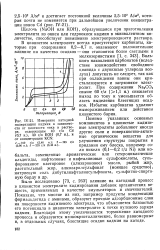 |
Измерение катодной поляризации кадмия в зависимости от плотности тока в растворе, содержащем 40 г / л Cd ( 0 7 н., 40 г / л КОН ( 0 7 н., и от концентрации KCN. [34] |
Показано, что многие из них, например продукты конденсации формальдегида с аминами, образуют прочные адсорбционные слои на поверхности кадмиевого электрода, что объясняется близостью его потенциала в цианистом электролите к точке нулевого заряда кадмия. Благодаря этому увеличивается торможение катодного процесса и образуются мелкокристаллические, более равномерные и, в отдельных случаях, блестящие осадки кадмия на катоде. [35]
Развитие щелевой коррозии связывают с затруднением доступа кислорода из объема электролита в зазор, изменением рН раствора электролита в зазоре и возникновением коррозионного элемента типа щель - открытая поверхность. Затруднение доступа кислорода вызывает торможение катодного процесса, в результате чего электродный потенциал металла в зазоре понижается и облегчается протекание анодного процесса. [36]
Поэтому при высоких частотах торможение катодного процесса разряда ионов водорода значительно меньше, чем при низких частотах. [37]
По мнению авторов работы [26], присутствующие в растворе ионы влияют не только на растворимость. Так, ионы цинка обеспечивают торможение катодного процесса на стали; хро-маты цинка, являясь основными, реагируют с высококислотными связующими; растворимые хлориды, сульфаты и нитраты уменьшают защитную способность хроматов, однако в присутствии ионов цинка это влияние ослабляется. [38]
Смещение потенциала электролиза в отрицательную сторону, если он соответствует предельному току, не влияет на характер поляризационных кривых. Это обусловлено, вероятно, торможением катодного процесса при изменении знака заряда поверхности электрода. В других случаях этот эффект не обнаружен. При потенциале предельного тока диффузии и равномерном перемешивании раствора или использовании вращающегося дискового электрода количество образующегося на электроде осадка пропорционально концентрации участвующих в процессе ионов и продолжительности электролиза. [39]
 |
Схема роста двухмерного зародыша. [40] |
Таким образом, процесс выделения металла на катоде протекает при увеличении, иногда весьма значительном, потенциала по сравнению с равновесным в электроотрицательную сторону для преодоления указанных торможений. Как будет показано ниже, величина и характер торможений катодного процесса играют большую роль в образовании металлических осадков той или иной структуры. [41]
Характер разъедания поверхности близок к равномерному. Уменьшение скорости коррозии при повышении температуры до 90 С объясняется преобладающим торможением катодного процесса вследствие уменьшения растворимости кислорода. [42]
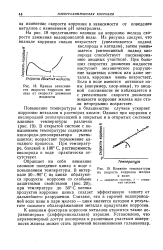 |
Кривая зависимости скорости коррозии железа от скорости движения жидкости.| Влияние температуры. [43] |
Повышение температуры в большинстве случаев ускоряет коррозию металлов в растворах кислот. В открытой системе с повышением температуры содержание кислорода-деполяризатора уменьшается; возрастает торможение катодного процесса. При температуре, близкой к 100 С, растворимость кислорода в воде практически отсутствует. [44]
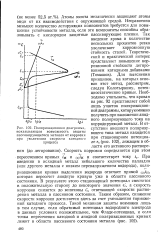 |
Поляризационная диаграмма, показывающая возможность защиты пассивирующегося металла от коррозии при увеличении скорости катодного процесса. [45] |
Страницы: 1 2 3 4 5