Увеличение - концентрация - азотная кислота
Cтраница 2
Стабильность сульфамината железа ( II) уменьшается с увеличением концентрации азотной кислоты. [16]
В растворах для химического полирования меди и ее сплавов увеличение концентрации азотной кислоты приводит к снижению светоотражательной способности обработанных поверхностей, а увеличение концентрации фосфорной кислоты ухудшает сглаживание. Корректирование полировального раствора ведется периодически, добавляя в него азотную кислоту и воду. [17]
Равновесие реакции (11.22) сдвигается в сторону образования С12 и N02 с увеличением концентрации азотной кислоты и температуры. Окисление NOC1 происходит в основном в жидкой фазе, вклад гомогенного окисления NOC1 азотной кислотой становится существенным [81] при температурах 160 - 300 С. [18]
В некоторых опытах М. И. Коновалов применял азотную кислоту и других концентраций; однако с увеличением концентрации азотной кислоты увеличивается количество образующихся полинитросоединений, а также продуктов окисления. С разбавлением азотной кислоты уменьшается образование побочных продуктов реакции, но снижается и нитрующая способность азотной кислоты. [19]
 |
Влияние нитрата алюминия на растворимость НЦГ в растворах азотной кислоты при различных температурах. [20] |
Растворимость НЦГ в растворах азотной кислоты, содержащих нитрат алюминия, увеличивается при увеличении концентрации азотной кислоты и температуры. [21]
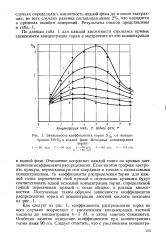 |
Зависимость коэффициента тория. Th от концентрации HNO3 в водной фазе. Исходные концентрации тория. [22] |
Как следует из рис. 1, коэффициенты распределения тория во всех случаях возрастают с увеличением концентрации азотной кислоты до концентрации 4 - 5 М, а затем заметно снижаются. [23]
Коэффициенты распределения так же, как и при экстракции из солянокислых растворов, уменьшаются при увеличении концентрации азотной кислоты, что может быть связано с конкурентной экстракцией азотной кислоты. [24]
Однако при использовании нитрометана кислотность водной фазы нельзя повышать более 5 5 N, поскольку с увеличением концентрации азотной кислоты в водной фазе возрастает растворимость нитрометана и примерно при 5 7 - 6 0 IV наступает полноз смешение фаз. В присутствии азотнокислых солей ( например нитрата кальция) растворимость нитрометана в водной фазе уменьшается. [25]
При изучении кинетики реакции окисления п-нитрозофе-нола в п-нйтрофенол Вайбель нашел, что скорость реакции сильно возрастает с увеличением концентрации азотной кислоты, но, с другой стороны, не зависит от концентраций нитро-зофенола и азотистой кислоты. Опыты показали, что окисление протекает нормально лишь в том случае, если имеется минимальная концентрация азотистой кислоты. [26]
При изучении кинетики реакции окисления тг-нитрозофе-нола в л-нитрофенол Вейбель нашел, что скорость реакции сильно возрастает с увеличением концентрации азотной кислоты, но, с другой стороны, не зависит от концентраций нитрозофенола и азотной кислоты. Опыты показали, что окисление протекает нормально лишь в том случае, если имеется минимальная концентрация азотистой кислоты. [27]
При изучении кинетики реакции окисления п-нитрозофе-нола в п-нйтрофенол Вайбель нашел, что скорость реакции сильно возрастает с увеличением концентрации азотной кислоты, но, с другой стороны, не зависит от концентраций нитро-зофенола и азотистой кислоты. Опыты показали, что окисление протекает нормально лишь в том случае, если имеется минимальная концентрация азотистой кислоты. [28]
Распределение нитрата тория между раствором азотной кислоты и диэтиловым эфиром впервые исследовано Имре [1098], показавшим, что увеличение концентрации азотной кислоты в водном слое приводит к повышению коэффициента распределения нитрата тория. Позднее было замечено, что насыщение водного слоя нитратами тория [1489] или некоторых металлов, не экстрагирующихся эфиром [398, 399, 783, 1741], значительно повышает коэффициенты распределения нитрата тория. [29]
 |
Давление пара HN03 в системе HN03 - Н3Р04 - Н20. [30] |
Страницы: 1 2 3 4