Увеличение - беспорядок
Cтраница 2
В изолированной системе все самопроизвольные процессы протекают в сторону увеличения беспорядка. Как изменяется при этом энтропия. [16]
Взаимодействия такого рода становятся менее вероятными при увеличении расстояний между частицами и при увеличении беспорядка в их расположении. В разбавленных растворах интерференцией можно обычно пренебречь; таким образом, рассеяние под малыми углами представляет собой сумму рассеяния, обусловленного отдельными частицами. [17]
 |
Изменение V, Н и СР при переходе вещества из фазы I во второе фазовое состояние II. [18] |
Это уравнение показывает, что процесс испарения связан с энергией разрыва межмолекулярных связей и увеличения беспорядка в системе. [19]
 |
При растворении твердого вещества в жидкости энтропия. [20] |
Мы можем даже сказать, что изменения происходят потому, что существует общая тенденция к увеличению беспорядка. Однако необходимо помнить, что этот обязательный рост энтропии характерен только для изолированных систем при постоянном объеме. [21]
Диспергирующим смешением называется процесс, в результате которого происходит как уменьшение размеров частиц, так и увеличение статистического беспорядка в их распределении. Примером подобного процесса служит введение технического углерода в полиэтилен. [22]
Диспергирующим смешением называется процесс, в результате: которого происходит как уменьшение размеров предельных частиц, так и увеличение статистического беспорядка в их распределении: Примером подобного процесса служит введение сажи в полиэтилен в смесителе Бенбери. В исходной смеси предельными частицами являются агломераты коллоидов сажи. В процессе диспергирующего смешения эти агломераты измельчаются на отдельные коллоидные частицы. При проведении анализа диспергирующего смешения возникают дополнительные трудности по сравнению с простым смешением, поскольку в этом случае следует учитывать природу и величину сил, необходимых для разрушения предельных частиц. [23]
Причина, почему теплота не может быть полностью превращена в механическую энергию, заключается в тенденции природы к увеличению беспорядка. Естественные процессы развиваются необратимо в направлении увеличения беспорядка, - так Больцман на основе молекулярного движения сформулировал второе начало термодинамики. Эта формулировка аналогична варианту второго начала, предложенному Клаузиусом; функцию состояния, энтропию, Больцман отождествил с мерой беспорядка. [24]
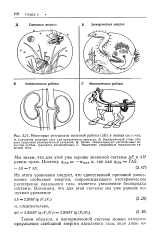 |
Некоторые результаты полезной работы ( ДО в живых системах. [25] |
Из этого уравнения следует, что единственной причиной уменьшения свободной энергии, сопровождающего изотермическое расширение идеального газа, является увеличение беспорядка системы. [26]
Поскольку теплоте присущ наиболее беспорядочный характер движения материи ( хаотическое движение молекул), можно сказать, что возрастание энтропии соответствует увеличению беспорядка в состоянии системы. [27]
 |
Тепловые эффекты реакций образования некоторых галогенидов щелочных металлов, QJ98 кДж / моль. [28] |
Теперь известно, что, помимо стремления к минимуму энергии, в физико-химических системах существует еще одна тенденция - стремление к увеличению беспорядка. [29]
Энергетический фактор энтальпии характеризует стремление частиц вещества к упорядочению, и, наоборот, энергетический фактор энтропии отражает стремление частиц вещества к увеличению беспорядка в расположении. [30]
Страницы: 1 2 3 4