Увеличение - энергия - активация
Cтраница 4
Так как атом азота становится все менее и менее способным к отдаче электронов, происходит увеличение энергии активации реакции, и константа скорости падает. Другой тип реакции, в которой наиболее важным является электростатическое взаимодействие между реагирующими молекулами, представляют обычные реакции замещения бензола ( стр. [46]
Прочность связи кислорода с поверхностью платины возрастает с повышением потенциала анода, что приводит к увеличению энергии активации ра спада поверхностных кислородных соединений и повышению перенапряжения кислорода. При потенциалах выше 2 0 В состояние поверхности платины меняется вследствие появления; хемосорбированных кислородных соединений радикального характера, образующихся дри разряде соответствующих анионов. [47]
 |
Кинетические параметры процесса окисления метилэтилкетона в смесях его с водой при 60 С. [48] |
В реакциях продолжения и обрыва цепи, протекающих с участием сольватированного водой радикала RC2, наблюдается увеличение энергии активации. Это не удивительно, если учесть, что теплота комплексообразования составляет 4 8 ккал / моль. Увеличение энергии активации в некоторой степени компенсируется уменьшением отрицательности энтропии активации. Вероятно, прежде, чем произойдет реакция сольватированных радикалов с RH или между собой, должен, произойти процесс десольватации. [49]
В ароматических растворителях ( бензол, этилбен-зол) в реакциях ряда стабильных радикалов с фенолами происходит увеличение энергии активации на 4 - 8 ккал / моль. Измеренные в работе [32] константы скорости гибели радикалов при их реакции с замещенным фенолом являются истинными константами взаимодействия радикала с молекулой, поскольку процессы с участием стабильных радикалов не осложнены побочными реакциями. Путем анализа кинетической схемы с участием несольватированного радикала и его л-комплекса в системе инертный растворитель - бензол была рассчитана константа равновесия комплексообразования радикала IV с бензолом. [50]
При адсорбции NH3 больше определенной величины наблюдается снижение энергии активации десорбции и вместе с тем происходит увеличение энергии активации реакции. Обе величины начинают изменяться в противоположные стороны примерно тогда, когда поверхность цеолита заполнена МН3 в количестве 0 2 ммоль / г. Последний факт еще раз подтверждает, что при данных условиях до степени покрытия - 0 2 ммоль / г адсорбция NH3 не оказывает влияния на каталитическую активность цеолита. Иначе говоря, в данном случае для катализа нужен лишь вырезанный участок спектра кислотности, причем очень сильные центры непосредственное участие в крекинге ку-мола не принимают. [51]
 |
Схематическое представление поверхности кристалла н положения атомов с различным числом атомов в первой и второй координационных сферах. [52] |
Наиболее правдоподобным объяснением является то, что атомы примеси взаимодействуют с поверхностными молекулами, что приводит к увеличению энергии активации испарения. Другим механизмом может быть медленная диффузия испаряемых молекул через пленку загрязнений, обусловливающая уменьшение скорости испарения. По этому вопросу имеется мало экспериментальных данных, поскольку при исследованиях скорости испарения стремятся избежать загрязнений поверхности. [53]
Видно, что слишком сильная адсорбция исходного вещества ( большая теплота адсорбции Саде) может привести к увеличению энергии активации каталитической реакции и к ее замедлению. [54]
Из сказанного следует, что увеличение факторов 1), 2) и 3) должно приводить к увеличению энергии активации реакции рассматриваемого типа, в то время как увеличение фактора 4) должно вызывать противоположный эффект. Первые три фактора можно назвать инерцией, а последний - движущей силой химической реакции. [55]
Показатель степени величины е RT отрицателен, следовательно, с повышением температуры скорость реакции возрастает, а с увеличением энергии активации уменьшается. Энергия активации процесса окисления SO2 в SO3 очень велика, и потому в отсутствие катализатора ( гомогенное окисление) реакция практически не идет даже при высокой температуре. В присутствии твердых катализаторов ( гетерогенный катализ) энергия активации понижается и скорость реакции возрастает. Таким образом, роль ванадиевой контактной массы как катализатора состоит в понижении энергии активации. [56]
Можно предположить, что при реакции с участием сольватированных молекул ( аналогично процессам с участием радикалов - комплексов) увеличение энергии активации вызвано необходимостью разрыва ассоциатов реагент - растворитель. Такая десольватация, предшествующая образованию переходного комплекса, приводит к разупорядочива-нию системы, результатом чего является увеличение энтропии активации. [57]
Если одинаковые молекулы подвергаются воздействию различных реагентов, заряды которых не сильно отличаются друг от друга, то, по мере увеличения энергии активации, заместители в атакуемой молекуле будут все в меньшей степени оказывать на нее то влияние, которое можно предвидеть, исходя из изменения отталкивающей способности реагента. [58]
Из этого уравнения следует, что уменьшение теплоты адсорбции и работы выхода или увеличение концентрации электронов в металле должно приводить к увеличению энергии активации и уменьшению скорости реакции. [59]
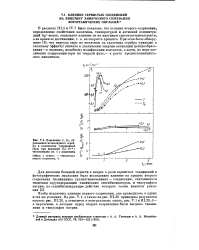 |
Изменение S, Do, образования негалоидного серебра и количества удержанной серы при введении 0 5 - 10 - г тиозиваыина на 1 г желатины. [60] |
Страницы: 1 2 3 4 5