Возрастание - концентрация
Cтраница 4
С возрастанием концентрации раствора поток воды уменьшается, а поток молекул летучего компонента увеличивается. При этом уменьшается время проскока и возникновения потока электролита. Проскок молекул HNO3 через мембрану даже из разбавленных растворов наблюдается и при незначительной глубине проникновения в объем фронта диффузии, отмечаемого по индикаторной границе. [47]
С возрастанием концентрации олефина уменьшается концентрация образующихся продуктов низкого и промежуточного молекулярного веса и димеров. В 1 % - ном растворе бутена [107] или октена [117] величина G этих продуктов при - 80 уменьшается на 0 2; 0 3 и 0 5 соответственно. За исключением димеров, эффект становится меньше при более высоких температурах. Для углеводородных продуктов уменьшение G, вызванное акцептированием олефинами, намного меньше, чем обусловленное иодом. [48]
С возрастанием концентрации раствора щелочи объем гранулы в Ме-форме уменьшается. Постоянная величина угла наклона прямых ( рис. 2) говорит, что разность осмотических давлений между раствором к ионитом изменяется пропорционально концентрации раствора. [49]
С возрастанием концентрации серной кислоты увеличивается количество бензолсуль-фоновой кислоты, образующейся вследствие расщепления связи Si-фенил. То обстоятельство, что с увеличением числа кислородных атомов в кремнийорганической молекуле увеличивается количество отщепившейся бензолсульфоновой кислоты, подтверждает ну-клеофильный механизм расщепления, предложенный Смантом, поскольку при электрофильном течении реакции кислородные атомы, напротив, понижают скорость расщепления. Из приведенных результатов можно сделать вывод, что для практических целей серная кислота не пригодна как среда для гидролиза метилфенилхлорсиланов или как реагент для каталитической перегруппировки с целью повышения молекулярного веса метилфенилполисилоксанов. [50]
С возрастанием концентрации раздражающего вещества С а уменьшается. [51]
С возрастанием концентрации хромовой кислоты наблюдается повышение анодной плотности тока и значительный рост толщины пленки. Максимальное значение толщины пленки соответствует концентрации раствора 30 г / л, после чего имеет место некоторое незначительное снижение, что связано с увеличением растворяющего действия электролита на пленку. [52]
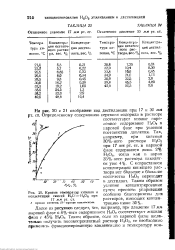 |
Кривые температур кипения и. [53] |
С возрастанием концентрации кипящего раствора все большие и большие количества НйОг переходят в дестиллат. [54]
С возрастанием концентрации серной кислоты ( при постоянных температуре и плотности тока) увеличивается скорость растворения окисла, вследствие чего уменьшается толщина пленки, образующейся за определенное время электролиза, и увеличивается пористость пленки. [55]
 |
Покрытие свинца пассивирующим слоем сульфата свинца.| Растворимость сульфата свинца в растворах серной кислоты. [56] |
С возрастанием концентрации серной кислоты растворимость сульфата свинца в ней уменьшается ( табл. 34), падает и скорость диффузии в основном из-за уменьшения градиента концентрации сульфата и увеличения вязкости раствора. Это также способствует образованию мелких кристаллов и усилению пассивации при разряде. Они становятся более мелкими и, следовательно, пассивация наступает раньше. Для уменьшения пассивации и повышения коэффициента использования активных масс разработан ряд мер. [57]
С возрастанием концентрации металлической ртути скорость реакции возрастает. [58]
 |
Зависимость концентрации СО2 ( / и NH3 ( 2 в жидкой фазе от концентрации NH3 в газовой фазе для плава синтеза с мольным CO ( NH2 a. Н2О 1 при 453 К н. [59] |
При возрастании концентрации NH3 в газовой фазе концентрация СО2 в жидкости уменьшается. [60]
Страницы: 1 2 3 4 5
