Феррит - натрий
Cтраница 4
Получение едкого натра по ферритному способу сводится к предварительному получению феррита натрия и последующему его разложению водой с выщелачиванием из спека едкого натра. [46]
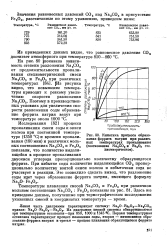 |
Кинетика процесса образования феррита натрия при различных температурах прокаливания ( соотношение Na2COs н Fe O3 сте-хиометрическое. [47] |
Поэтому в производственных условиях для увеличения скорости разложения соды образование феррита натрия ведут при температуре около 1000 С. [48]
В качестве примеров можно привести выщелачивание едкого натра из спека феррита натрия, сернистых натрия и бария из плавов, алюмината натрия в производстве глинозема методом спекания. [49]
Режим работы аппарата для гашения характеризуется следующими показателями: температура поступающего феррита натрия 900 - 950 С, температура гашеного феррита 105 - 110 С. [50]
Ими экспериментально показано, что соединение К20 6Fe203 существует, а аналогичный феррит натрия состава Na20 6Fe203 не образуется. [51]
С повышением температуры выщелачивания увеличивается скорость растворения алюмината натрия и разложения феррита натрия, а продолжительность процесса сокращается. Однако одновременно ускоряются и вторичные реакции, связанные с разложением двухкальциевого силиката. При 50 - 70 С двухкальциевый силикат разлагается сравнительно медленно, при температуре выше 90 С скорость его разложения значительна. [52]
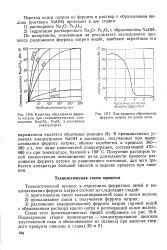 |
Кинетика образования феррита натрия при стехиометрическом соотношении Na2CO3. Рв2О3 и различных температурах.| Ход процесса образования феррита натрия по длине печи. [53] |
В промышленных условиях концентрация NaOH в растворах, получаемых при выщелачивании феррита натрия, обычно колеблется в пределах 360 - 380 г / л, что ниже равновесной концентрации, составляющей 470 - 480 г / л при температуре, близкой к 100 С. Получение растворов такой концентрации неэкономично из-за длительности процесса разложения феррита натрия до равновесного состояния, для чего требуется аппаратура большой емкости и ведение процесса при кипении. [54]
Страницы: 1 2 3 4