Восстановление - комплексный ион
Cтраница 1
Восстановление комплексного иона происходит при более сильной катодной поляризации электрода, и комплексообразование связано со сдвигом потенциала восстановления в сторону более отрицательных значений. [1]
Смещение потенциалов восстановления комплексных ионов относительно потенциалов восстановления простых ионов можно особенно легко описать в случае, когда в растворе присутствует только один комплексный ион состава MeLp, причем устойчивость этого иона большая. [2]
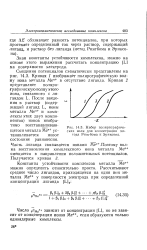 |
Набор полярографических волн для иллюстрации метода Рингбома и Эриксона. [3] |
Поэтому волна восстановления комплексного иона металла Мел смещается в направлении положительных потенциалов. [4]
Более сложные превращения при восстановлении комплексных ионов рассмотрены в [ 2; 11, с. [5]
 |
Потенциалы полуволн восстановления комплексных соединений никеля. [6] |
Следует иметь в виду, что потенциалы полуволн восстановления комплексных ионов металлов отличаются от потенциалов полуволн простых ионов и зависят от констант устойчивости комплекса. [7]
Отсутствие прямой связи между константой равновесия и величиной перенапряжения при восстановлении комплексных ионов металла [37, 38] дает основание предполагать, что и в случае аква-комплекса прочность его также не должна оказывать существенного влияния на протекание электродного процесса. [8]
Хорошо выраженные катодные полярограммы никеля на графитовом электроде могут быть получены лишь при восстановлении комплексных ионов металла. [10]
Значения величин а и b в этом выражении отражают две совместно протекающие элбктровсимииесиие реакции - восстановление комплексного иона с выделением меди и разряд ионов водорода. [11]
При избытке реактива в растворе можно с известным приближением считать, что его количество в приэлектродном слое не зависит от протекания реакции восстановления комплексного иона. [12]
При избытке реактива в растворе можно с известным приближением считать, что его количество в приэлектродном слое не зависит от протекания реакции восстановления комплексного иона. [13]
Изучение процесса электроосаждения серебра из цианистых растворов позволяет рассмотреть одну из важных проблем электрохимии, а именно, каким образом происходит выделение металла, находящегося в растворе в виде комплексного иона: путем восстановления свободного катиона металла или непосредственно за счет восстановления комплексного иона. [14]
Необходимо отметить интересную особенность влияния комп-лексообразователей на восстановление никеля и кобальта. Для большинства катионов восстановление комплексных ионов происходит при более отрицательных потенциалах, чем восстановление простых ( гидратированных) ионов. Однако для никеля и кобальта наблюдается обратная зависимость: потенциалы полуволн становятся более положительными при введении комплексо-образователей. Это явление объясняется тем, что гидратированные ионы никеля и кобальта ( в растворе хлористого калия) восстанавливаются необратимо с большим перенапряжением. Перевод этих ионов в комплексные ионы устраняет перенапряжение и сдвигает полярографические волны в область более положительных потенциалов. [15]
Страницы: 1 2