Электролиз
Cтраница 4
Электролиз NaN03 вследствие малой его проводимости не дал столь ощутимых результатов; однако с полной несомненностью нам удалось с помощью лакмусовой бумажки обнаружить щелочную реакцию на катодном слое кристалла и на служившей катодом платиновой пластинке, что свидетельствует о накоплении Na у катода. [46]
Электролиз осуществляется при пропускании через воду электрического тока. Этот способ отличается высоким КПД, определяемым как отношение теплоты сгорания полученного топлива к энергозатратам на выделение Н2 и О2 при электролизе воды и достигающим 70 - 80 % и более. [47]
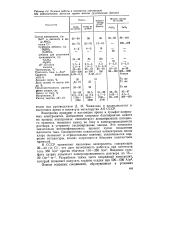 |
Условия работы и показатели электролиза. [48] |
Электролиз проводят в настоящее время в сульфат-хлорид-ных электролитах. Добавление хлоридов благоприятно влияет на процесс электролиза: способствует деполяризации катодного процесса, повышает выход по току и электропроводимости раствора и устраняет пассивирование анодов. Это позволяет значительно интенсифицировать процесс путем повышения плотности тока. Одновременно повышенная концентрация ионов хлора оказывает и отрицательное влияние: увеличивается коррозия аппаратуры, анолит загрязняется большим количеством примесей. [49]
Электролиз с нерастворимыми анодами в последнее время привлекает пристальное внимание для получения никеля. Исходным сырьем служит дважды конвертированный штейн, из которого сера удалена настолько, что в виде сульфида остается только медь. Никель присутствует в виде металла. Этот материал выщелачивают кислым отработанным анолитом электролизных ванн, которые работают с анодами из свинца. [50]
Электролиз ведется несколькими последовательными стадиями. Для повышения электропроводности воды к ней прибавляют щелочь, концентрация которой увеличивается по мере разложения воды. После того как концентрация щелочи увеличится в 10 - 15 раз, электролиз останавливают, нейтрализуют щелочь угольным ангидридом и снова повторяют электролиз. [51]
Электролиз проводят при высокой скорости протекания электролита через каскад из 8 - 9 блоков ванн ( см. рис. 4.13), чтобы предотвратить значительное окисление железа на нерастворимом аноде, обладающем высоким электроположительным потенциалом. [52]
Электролиз при более отрицательном потенциале сопровождается уменьшением тока электрохимического растворения металла. [53]
Электролиз в азотнокислом растворе очень длителен. Более быстро процесс протекает в сернокислом растворе. Однако некоторое количество азотной кислоты как деполяризатора необходимо в этом случае. Иначе получается красный и менее блестящий осадок меди. Раствор во всех случаях не должен содержать азотистую кислоту, замедляющую выделение меди и вызывающую образование закиси или окиси меди. [54]
Страницы: 1 2 3 4