Выход - реакция
Cтраница 3
Выход реакции обычно значительно ниже теоретического ( найденного стехиометрическим расчетом) по следующим причинам: 1) обычно перед достижением состояния равновесия реакция получения целевого продукта прерывается ( разность скоростей прямой и обратной реакций очень мала); 2) главной реакции часто сопутствуют побочные, приводящие к увеличению расхода исходных веществ; 3) в технологическом процессе существуют различные потери, не учтенные в теоретическом расчете. [31]
Выход реакции в объем при окислении насыщенных углеводородов на платине не изучен. Доля объемного продолжения реакции в этом случае, вероятно, должна быть значительно больше, чем для непредельных углеводородов, так как при адсорбции таких углеводородов образуются два радикала на поверхности контакта и один из них легко может перейти в объем. Еще более вероятным следует считать взаимодействие радикала с кислородом газовой фазы с отрывом от образующегося соединения на поверхности контакта перекисного радикала и продолжением реакции в объеме. [32]
Выход реакции D ( d, n) 3He велик. Он соответствует выходу нейтронов от источника ( 50 г Ra Be) на миллиампер дейтонно-го тока при Ed0 2 Мэв и достигает максимума при Е - 1 5 Мэв. Реакция D ( d, n) 3Не особенно существенна как источник монохроматических нейтронов с энергией от 2 до 10 Мэв. [33]
Выход реакции ацетилирования определяют путем омыления навески полученного продукта. Далее от полученного продукта отгоняют при температуре до 65 ( 5 мм) 30 г легкокинящей фракции и оставшийся продукт омыляют путем нагревания с водно-спиртовым раствором едкого кали. [34]
Выход реакции образования перекиси водорода может быть определен из линейной части кинетической кривой, которая характеризует скорость прямой реакции и составляет для у-излучения - - 1 7 экв. [35]
Выход реакции образования окиси азота зависит и от соотношения концентрации азота и кислорода в реагирующей смеси. Наиболее благоприятным является такое соотношение, когда на каждую грамм-молекулу азота приходится одна грамм-молекула кислорода. [36]
Выход реакции образования окиси азота зависит и от соотношения концентрации азота и кислорсда в реагирующей смеси. Наиболее благоприятным является такое соотношение, когда на каждую грамм-молекулу азота приходится одна грамм-молекула кислорода. [37]
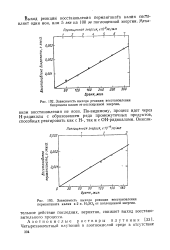 |
Зависимость выхода реакции восстановления бихромата калия от поглощенной энергии. [38] |
Выход реакций восстановления перманганата калия составляет один ион, или 5 же на 100 эв поглощенной энергии. [39]
Выходом реакции называется отношение количества получаемого вещества к тому его количеству, которое получилось бы при протекании реакции до конца. [40]
Выходом реакции называется отношение количества получаемого вещества г. тому его количеству, которое получилось бы при протекании реакции до конца. [41]
Выходом реакции называется отношение количества получаемого вещества к тому его количеству, которое получилось бы при протекании реакции до конца. [42]
Выходом реакции называется отношение количества получаемого вещества к тому его количеству, которое получилось бы при протекании реак-лии до конца. [43]
Выходом реакции называется отношение количества получаемого вещества к тому его количеству, которое образовалось бы при протекании реакции до конца. [44]
Выходом реакции называется доля одного из исходных веществ, вступивших в реакцию, или мольная доля продукта реакции в равновесной смеси. Таким образом, в равновесной смеси остается 74 % непро - реагировавшего - азота. [45]
Страницы: 1 2 3 4